5.3 Nomenclatura tradizionale
QUIZ 10
Medicina 1998
I pesi atomici di H, P ed O sono rispettivamente 1, 31 e 16 u.m.a. Il peso molecolare espresso in u.m.a. dell' acido ortofosforico è:
Per rispondere al quiz dobbiamo conoscere la nomenclatura della chimica inorganica.
In generale per ottenere un ossiacido facciamo reagire una anidride con una molecola d’acqua. In alcuni casi però la reazione può avvenire sommando anche due o tre molecole d’acqua ottenendo diversi ossiacidi. Per distinguerli si usa il prefisso meta-, piro- e orto-. Il caso tipico richiesto a volte nei quiz si ha con l’anidride fosforica.
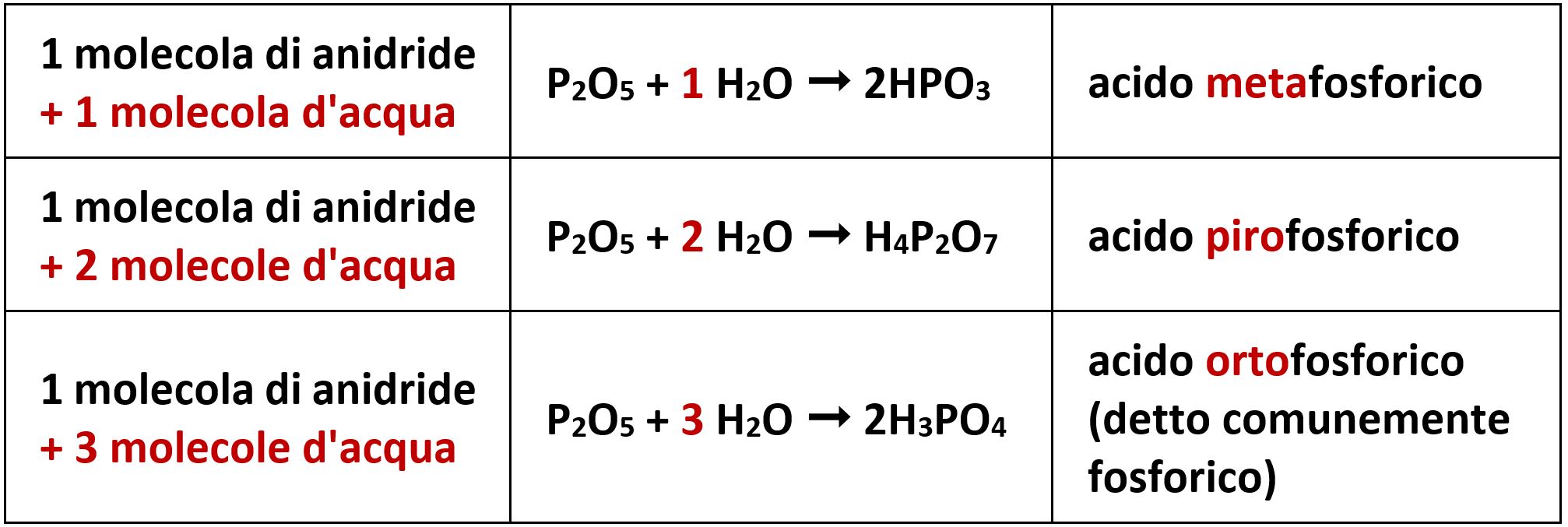
Si tratta così di H3PO4.
il peso molecolare ci calcola facilmente considerando il peso atomico di tre atomi di idrogeno, uno di fosforo e quattro di ossigeno:
3•1 + 31 +4•16 = 98 uma
QUIZ sulla Nomenclatura tradizionale |
|||
|---|---|---|---|
© il testo è di esclusiva proprietà dell’autore ed è sottoposto a COPYRIGHT – non è consentito alcun utilizzo diverso dallo studio gratuito degli utenti del sito


