1.1 La Materia
Chiamiamo “sistema” una porzione di materia dell’universo.
Nel capitolo 7 analizziamo i sistemi in funzione degli scambi con l’ambiente di materia e di energia.
La Chimica prende in esame un sistema e ne studia:
- La composizione (struttura)
- le trasformazioni della sua composizione
- l’energia in gioco durante la trasformazione
Un sistema può essere omogeneo o eterogeneo sia a livello fisico che a livello chimico.
1.1.1 Sistemi fisicamente omogenei ed eterogenei
A livello fisico un sistema omogeneo possiede un’unica consistenza, in termini tecnici possiamo dire che è composto da un’unica fase. Ad esempio l’acqua contenuta in un bicchiere è composta da un’ unica fase acquosa ed è per questo un sistema fisicamente omogeneo. Anche un cubetto di ghiaccio considerato da solo è composto da un’unica fase ed è un sistema fisicamente omogeneo. Se invece consideriamo un sistema costituito da una certa quantità d’acqua insieme a del ghiaccio galleggiante ed anche l’aria sovrastante contenente vapore acqueo, avremo un sistema fisicamente eterogeneo composto da tre fasi.
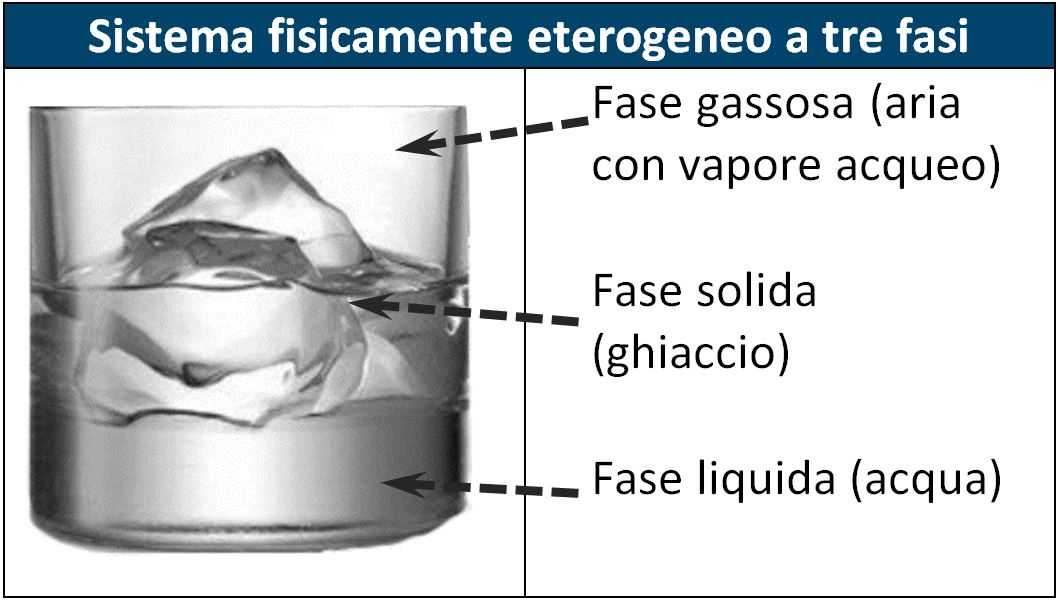
| ! | Una miscela di gas, anche se di natura profondamente diversa, costituisce sempre un’unica fase. |
1.1.2 Sistemi chimicamente omogenei ed eterogenei
Per l’individuazione della natura chimica del sistema facciamo riferimento al concetto di sostanza. Quando parliamo di una sostanza intendiamo una porzione di materia omogenea in ogni punto sia per proprietà fisiche che chimiche. Una sostanza è ad esempio l’ossigeno gassoso costituito solamente da molecole di O2 oppure l’acqua costituita da molecole identiche del composto chimico H2O. C’è una differenza tra le due sostanze O2 e H2O. Nelle molecole di ossigeno O2 troviamo atomi di un solo elemento chimico e per questo motivo lo definiamo una sostanza pura. Al contrario nell’acqua H2O troviamo atomi diversi, due di idrogeno ed uno di ossigeno e per questo la definiamo un composto.
A seconda del contesto le sostanze pure come l’ossigeno O2, l’idrogeno H2 o l’azoto N2 vengono chiamate con il nome di “elementi”. Altre volte il termine “elemento” viene utilizzato per indicare uno specifico elemento della tavola periodica; dipende dal contesto.
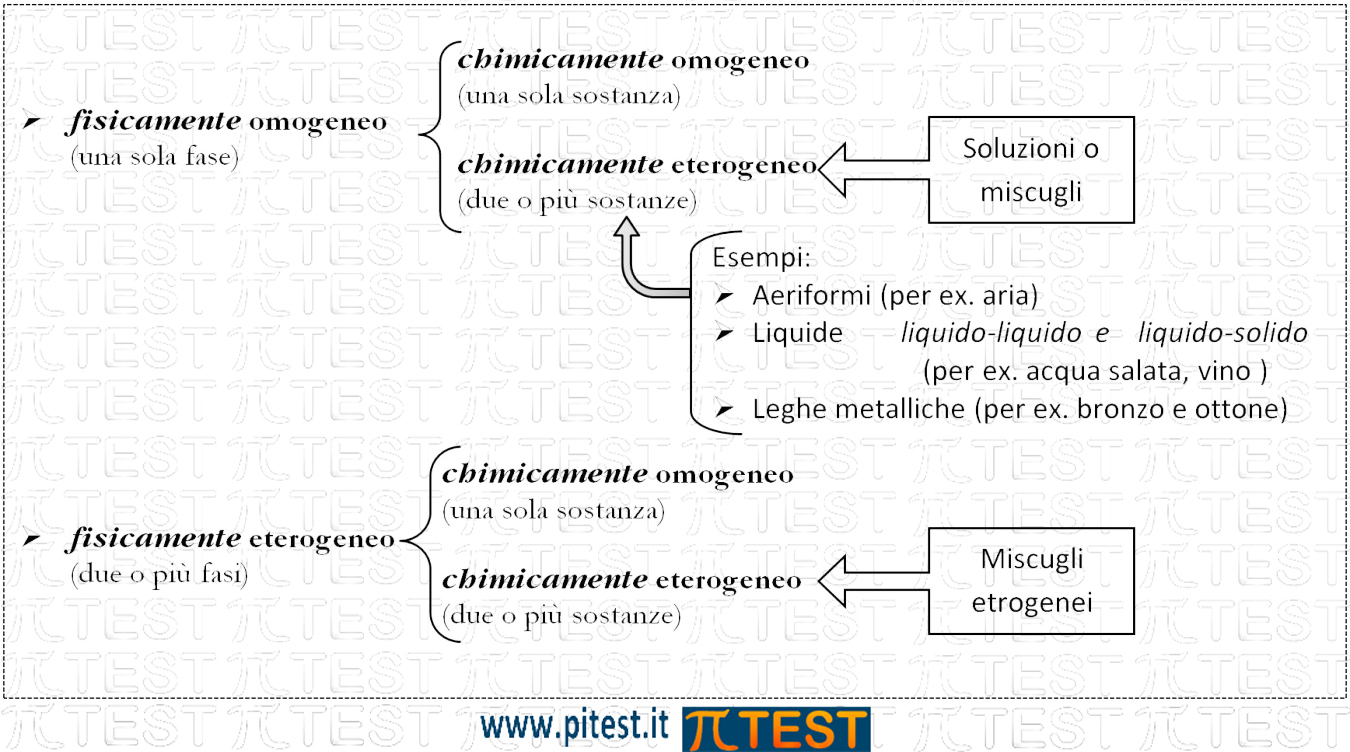
Un sistema si definisce chimicamente omogeneo se è costituito da una sola sostanza. Se invece è costituito da due o più sostanze risulta chimicamente eterogeneo.
Un sistema chimicamente eterogeneo è chiamato miscuglio. Quando un miscuglio è fisicamente omogeneo è chiamato anche soluzione, ad esempio acqua con un sale disciolto.
| ! | Le soluzioni, o miscugli omogenei costituiscono un sistema fisicamente omogeneo e chimicamente eterogeneo. |
Esempi:
- un sistema costituito da acqua con ghiaccio galleggiante è fisicamente eterogeneo perché possiede due fasi distinte, ma è chimicamente omogeneo in quanto è costituito dalla stessa sostanza, l’acqua.
- Acqua ed olio sono un sistema chimicamente eterogeneo e fisicamente eterogeneo in quanto sono presenti due fasi liquide distinte separate.
1.1.3 Colloidi
Una attenzione particolare va posta ai colloidi che sono sistemi nei quali in una fase continua troviamo una fase dispersa con una dimensione con valori compresi tra 1μm (micrometro o micron pari a 10‒6m) e 1 nm (nanometro pari a 10‒9m).
Nello schema seguente vengono date le esatte definizioni delle dispersioni, dei colloidi e delle Soluzioni.
Anche se finora i quiz dei test di ammissione alle facoltà medico-sanitarie non hanno riguardato i colloidi, è opportuno conoscerne la natura perché non possiamo escludere che vengano richiesti.
|
Fisicamente eterogeneo (due o più fasi) |
Fisicamente omogeneo (una sola fase) |
||||
|
10‒6m 1 μm |
10‒9m 1 nm |
||||
| Dispersioni | Colloidi | Soluzioni | |||
| Una sospensione è una dispersione; una miscela eterogenea in cui una fase dispersa solida con dimensione particellare >1μm è disciolta in una fase disperdente (o continua) liquida, non in grado di sedimentare in tempo breve.
Le sospensioni più comuni sono quelle di solidi in acqua; alcuni esempi sono: Succo di frutta: polpa di frutta in acqua. Fango: terra, argilla e limo in acqua. Gelatina: acqua in una matrice di proteine. Gelato: cristalli di ghiaccio in crema |
colloidale) è una particolare miscela in cui una sostanza si trova in uno stato finemente disperso, intermedio tra la soluzione e la dispersione. Questo stato “microeterogeneo” consiste quindi di due fasi: una fase costituita da una sostanza di dimensioni microscopiche (diametro da 1 nm a 1 μm) e una fase continua disperdente.
Esempi: burro, maionese, asfalto, colla, nebbia e fumo |
Una soluzione è una miscela omogenea in cui una o più sostanze sono contenute in una fase liquida o solida o gassosa; contiene particelle diverse mescolate e distribuite in modo uniforme nello spazio disponibile in modo che ogni volume di soluzione abbia la medesima composizione degli altri. | |||
Alcuni colloidi
| Fase dispersa | Fase continua | Nome | Esempio |
| Liquido | Gas | Aerosol liquido | Nebbia, spray liquidi |
| Solido | Gas | Aerosol solido | Fumo, particolato, polvere |
| Gas | Liquido | Schiuma | Schiuma da barba, panna montata |
| Liquido | Liquido | Emulsione | Latte, maionese, sangue |
| Solido | Liquido | Sol | Pasta dentifricia |
| Gas | Solido | Schiuma solida Spugna | Polistirene o poliuretano espansi |
| Liquido | Solido | Gel | Opale, formaggio |
| Solido | Solido | Sospensione solida | Plastiche pigmentate, vetro, leghe metalliche |
Casi particolari
| Latte | È un miscuglio chimicamente eterogeneo (diversi composti chimici) e fisicamente eterogeneo (particelle grasse come il burro in fase liquida separate dalla fase liquida acquosa) |
| Fumo | È un sistema fisicamente eterogeneo in quanto è presente una polvere sottilissima (solida, anche se di piccole dimensioni) dispersa, sospesa, nella fase aeriforme. L’aria con “particolato” è un tipo di fumo originato dall’inquinamento. |
| Nebbia | È un sistema chimicamente eterogeneo (aria + particelle del liquido) e fisicamente eterogeneo in quanto è presente una fase liquida con particelle di piccolissime dimensioni dispersa nella fase aeriforme. La definizione esatta di una nebbia è “concentrazione sovrassatura metastabile di un liquido in una fase aeriforme”. |
| Lega metallica | È un sistema fisicamente omogeneo. Diversi metalli sono distribuiti nella fase solida senza alcuna discontinuità. |
© il testo è di esclusiva proprietà dell’autore ed è sottoposto a COPYRIGHT – non è consentito alcun utilizzo diverso dallo studio gratuito degli utenti del sito
QUIZ 1.1 La materia |
|||
|---|---|---|---|


