10.6.15 AMMINE
Le ammine sono composti organici contenenti azoto. Possiamo immaginarle partendo da una molecola di ammoniaca nella quale possiamo sostituire uno o più atomi di idrogeno con un radicale organico alchilico o arilico.
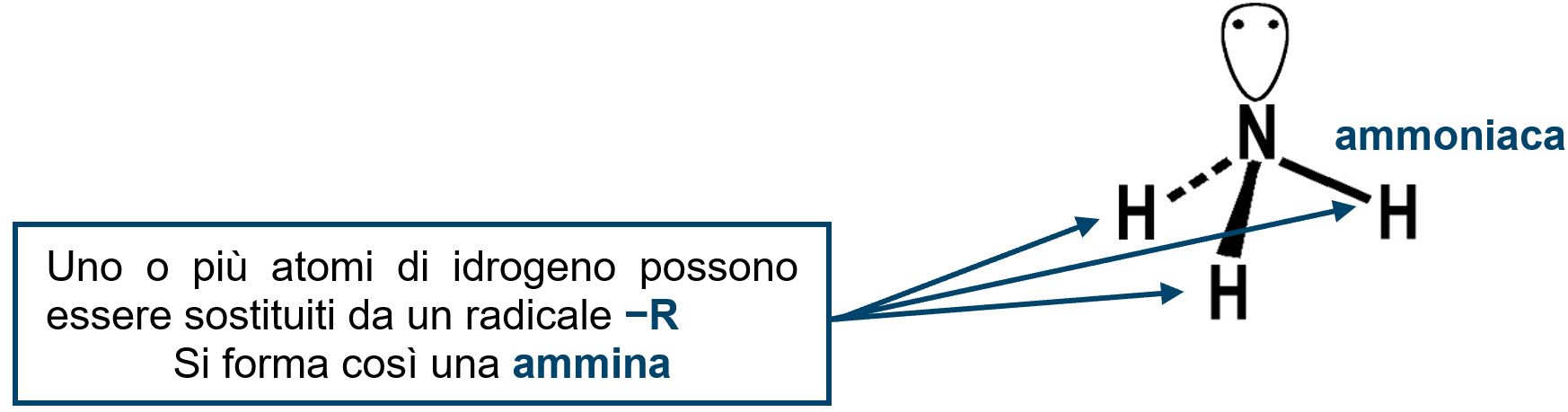
A seconda che siano presenti uno, due o tre radicali le ammine sono classificate col nome di primaria, secondarie o terziarie.
|
|
|
|
| Formule di struttura | |||
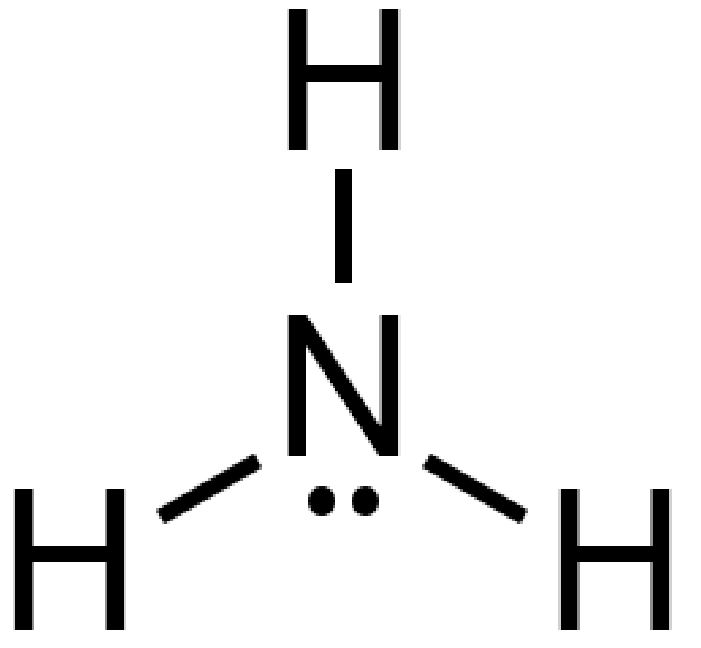 Ammoniaca Ammoniaca |
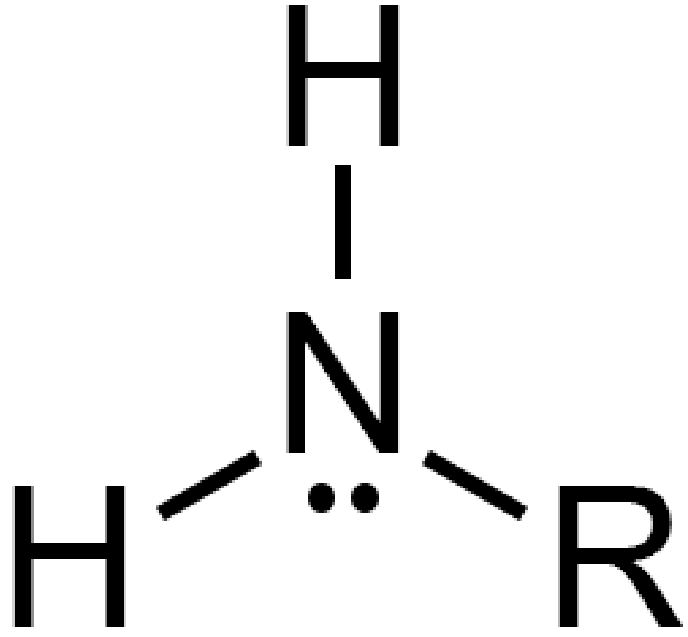 Ammina primaria Ammina primaria |
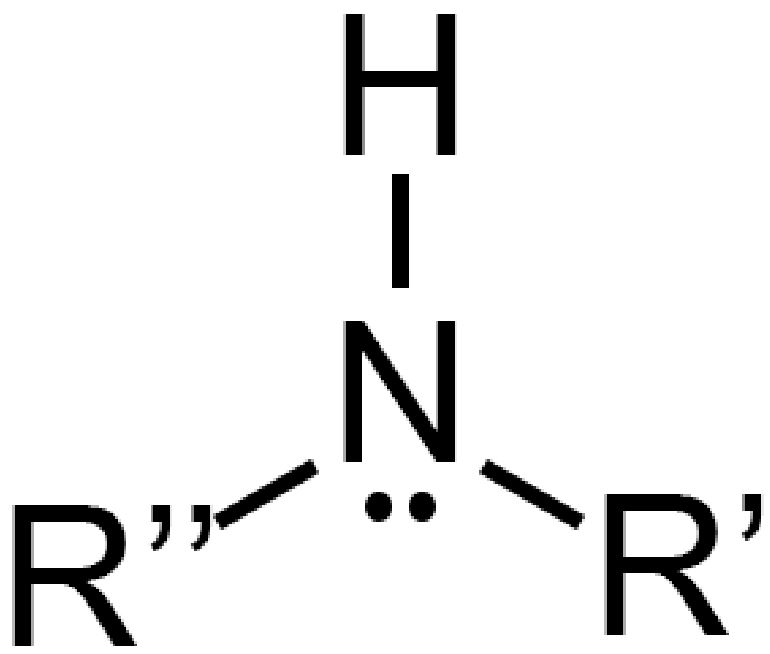 Ammina secondaria Ammina secondaria |
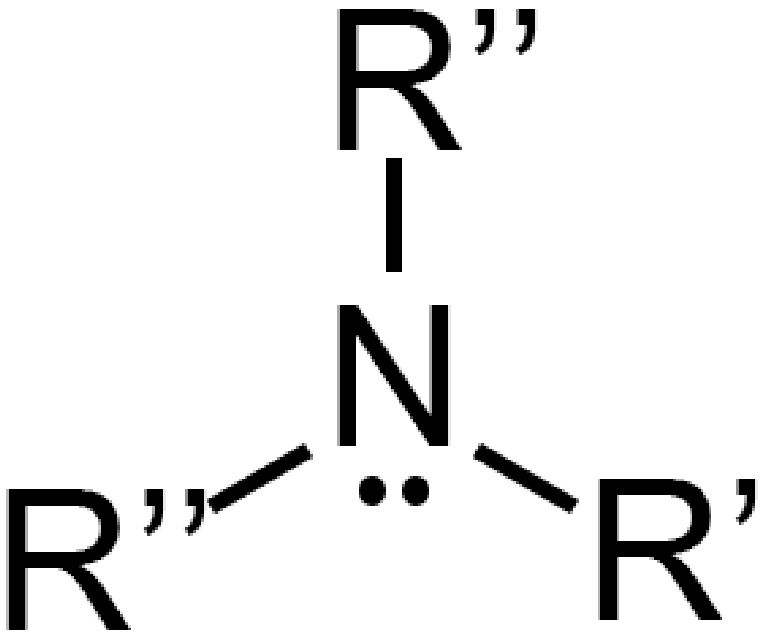 Ammina terziaria Ammina terziaria |
NATURA BASICA DELLE AMMINE
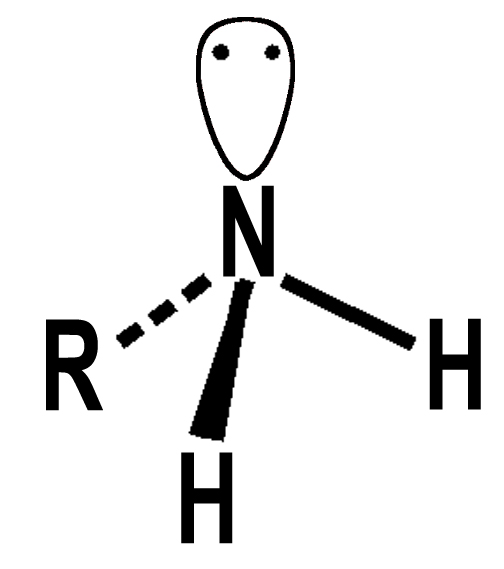
La natura basica dell’ammoniaca dovuta al doppietto libero (vedi) rimane anche nelle ammine.

LEGAMI INTERMOLECOLARI DELLE AMMINE
Abbiamo visto che l’ammoniaca può avere legami idrogeno (ponti idrogeno) tra il doppietto libero di una molecola e l’idrogeno di un’altra molecola (vedi). La stessa cosa accade anche per le ammine primarie e secondarie. Le ammine terziarie però non possiedono più atomi di idrogeno legati all’azoto e per questo motivo le ammine terziarie possono formare legami idrogeno con altre molecole come l’acqua, l’ammoniaca o un alcol, ma non tra di loro.
La presenza di legami idrogeno, legami intermolecolari molto forti, conferisce alle ammine una bassa volatilità, ovvero punti di ebollizione alti.
AMMINE QUATERNARIE
| Se facciamo riferimento allo ione ammonio NH4+, comprendiamo anche la possibilità di avere ammine con quattro radicali. Similmente allo ione ammonio risulteranno cariche positivamente e per questo si trovano in natura come sali. |
|
ANILINA
| Ricordiamo, tra le tante ammine esistenti, l’anilina. È una ammina primaria con un radicale fenilico |
|
10.6.16 AMMIDI
Sono composti quaternari caratterizzati dal gruppo funzionale RCONH2 .
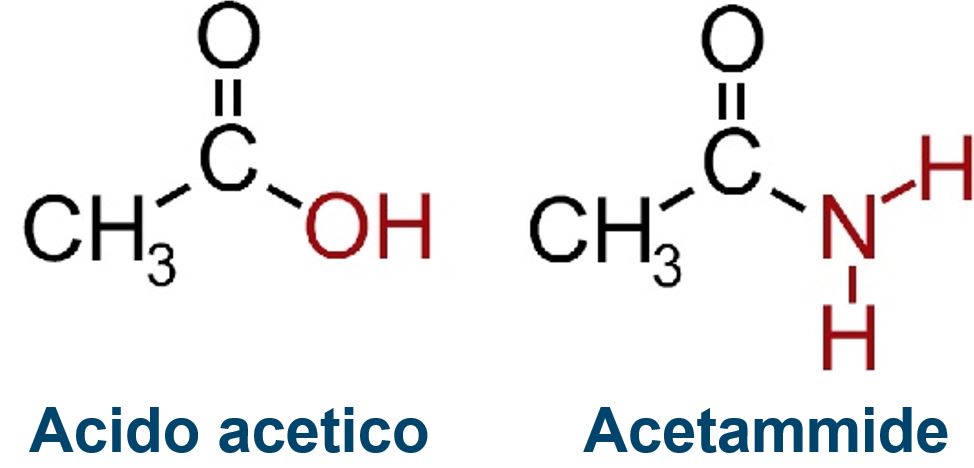
Per comprendere e ricordare la struttura immaginiamo di partire da un acido carbossilico e sostituire il gruppo −OH con una ammina.
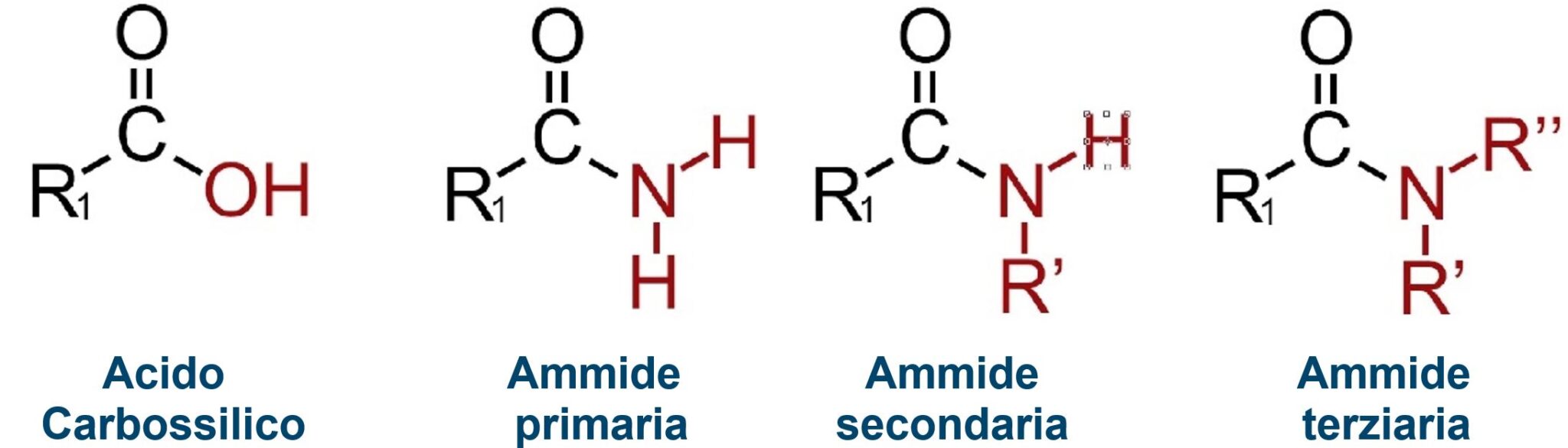
Per quanto riguarda la nomenclatura ricordiamo che prendono il nome dall’acido carbossilico corrispondente.
© il testo è di esclusiva proprietà dell’autore ed è sottoposto a COPYRIGHT – non è consentito alcun utilizzo diverso dallo studio gratuito degli utenti del sito
CONTINUA LO STUDIO DELLA CHIMICA ORGANICA
10.1 Idrocarburi
10.2 Idrocarburi alifatici
10.2.1 Idrocarburi alifatici saturi: gli ALCANI
10.2.2 Radicali alchilici
10.2.3 Idrocarburi ramificati
10.2.4 Proprietà fisiche e chimiche degli alcani
10.2.5 Idrocarburi insaturi: ALCHENI
10.2.6 Proprietà fisiche e chimiche degli alcheni
10.2.7 Idrocarburi insaturi: ALCHINI
10.2.8 Proprietà fisiche e chimiche degli alchini
10.2.9 POLIENI
10.2.10 CICLOALCANI, CICLOALCHENI E COCLOALCHINI
10.2.11 Composti ETEROCICLICI SATURI
10.3 Gli isomeri
10.3.1 Isomeri COSTITUZIONALI DI CATENA
10.3.2 Isomeri COSTITUZIONALI DI POSIZIONE
10.3.3 Isomeri COSTITUZIONALI DI FUNZIONE
10.3.4 Stereoisomeri CONFORMAZIONALI
10.3.5 Stereoisomeri CONFIGURAZIONALI GEOMETRICI
10.3.6 Stereoisomeri CONFIGURAZIONALI OTTICI
10.4 IDROCARBURI AROMATICI
10.4.1 BENZENE
10.4.2 I PRINCIPALI COMPOSTI AROMATICI DERIVANTI DAL BENZENE ‒ ARENI
10.4.3 IDROCARBURI POLICICLICI AROMATICI
10.4.4 COMPOSTI ETEROCICLICI INSATURI
10.5 ADDIZIONE E SOSTITUZIONE ELETTROFILA
10.5.1 ADDIZIONE ELETTROFILA
10.5.2 SOSTITUZIONE ELETTROFILA
10.6 GRUPPI FUNZIONALI
10.6.1 ALOGENURI ALCHILICI E ARILICI
10.6.3 ALCOLI
10.6.4 Proprietà fisiche e chimiche e preparazione degli ALCOL
10.6.5 POLIALCOLI (POLIOLI)
10.6.6 ETERI
10.6.7 CARBONILE – ALDEIDI E CHETONI
10.6.8 CARBOSSILE – ACIDI ORGANICI
10.6.9 ANIDRIDI
10.6.10 ESTERI
10.6.11 LIVELLI DI OSSIDAZIONE DELLE MOLECOLE ORGANICHE
10.6.12 SAPONIFICAZIONE
10.6.13 FOSFOLIPIDI
10.6.14 LIPIDI O GRASSI
10.6.15 AMMINE
10.6.16 AMMIDI
10.6.17 AMMINOACIDI – PROTEINE
10.7 POLIMERI
10.8 CARBOIDRATI


 Ammina primaria
Ammina primaria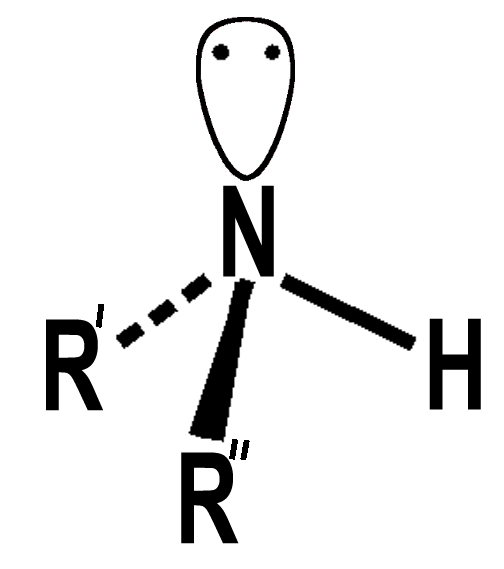 Ammina secondaria
Ammina secondaria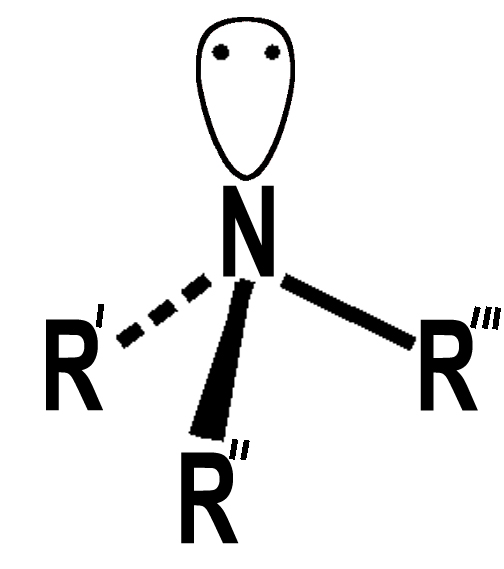 Ammina terziaria
Ammina terziaria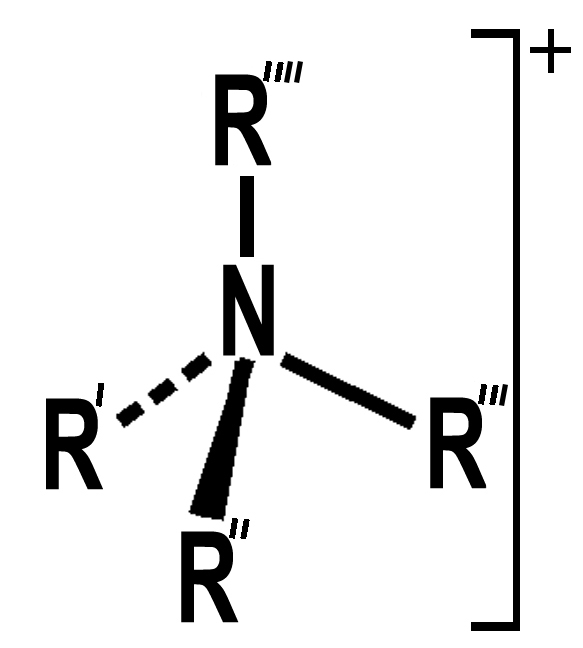 Ammina quaternaria
Ammina quaternaria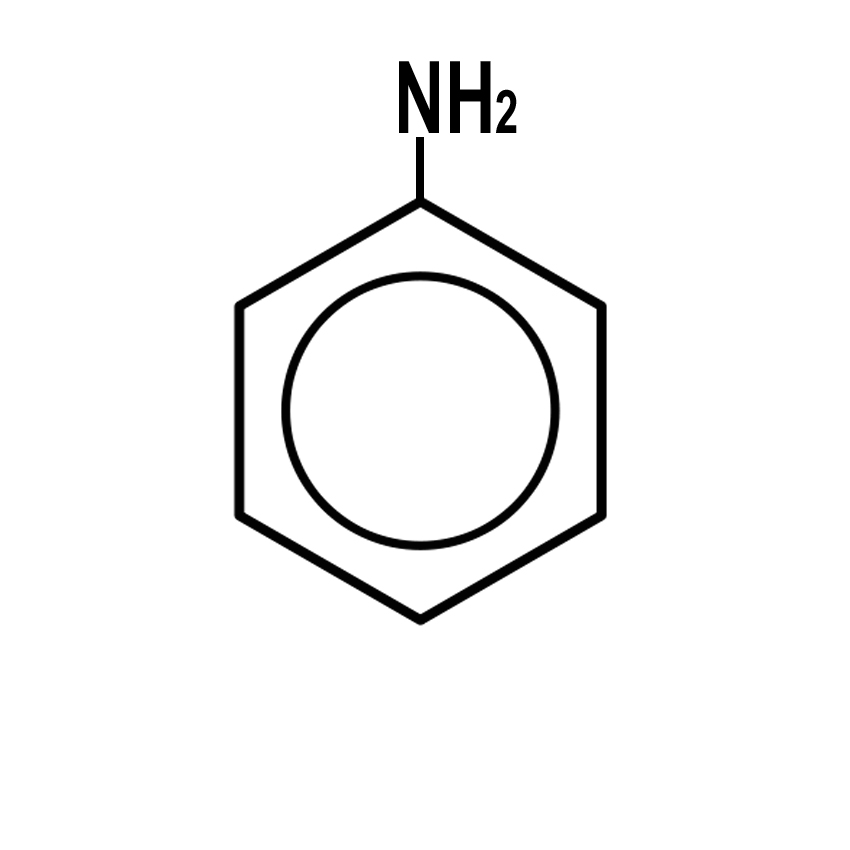 Anilina
Anilina