10.5 ADDIZIONE E SOSTITUZIONE ELETTROFILA
In chimica organica sono state individuate tantissime reazioni andandole a studiare lungo tutti i passaggi che, partendo dai reagenti, portano ai prodotti. Sono stati studiati gli effetti che i vari radicali e i diversi gruppi funzionali esplicano nei confronti delle parti di molecola interessate ai cambiamenti strutturali. Nella classificazione delle reazioni chimiche sono state individuate le reazioni di addizione elettrofila e di sostituzione elettrofila, razioni che vengono chieste, a volte, nei quiz dei test di ammissione.
In queste reazioni una molecola organica che presenta uno o più doppi legami incontra un’altra molecola che chiamiamo elettrofila, perché possiede una zona dotata di carica positiva (polarizzazione permanente o polarizzazione momentanea). Un tipico esempio è la molecola di acido cloridrico HCl che possiede sull’atomo di idrogeno un forte polo positivo.
10.5.1 ADDIZIONE ELETTROFILA
Un idrocarburo insaturo (tipicamente un alchene) nel secondo legame π possiede due zone che, viste da vicino, sono fortemente negative. L’agente elettrofilo attacca, urtandolo, il legame π provocandone la rottura.
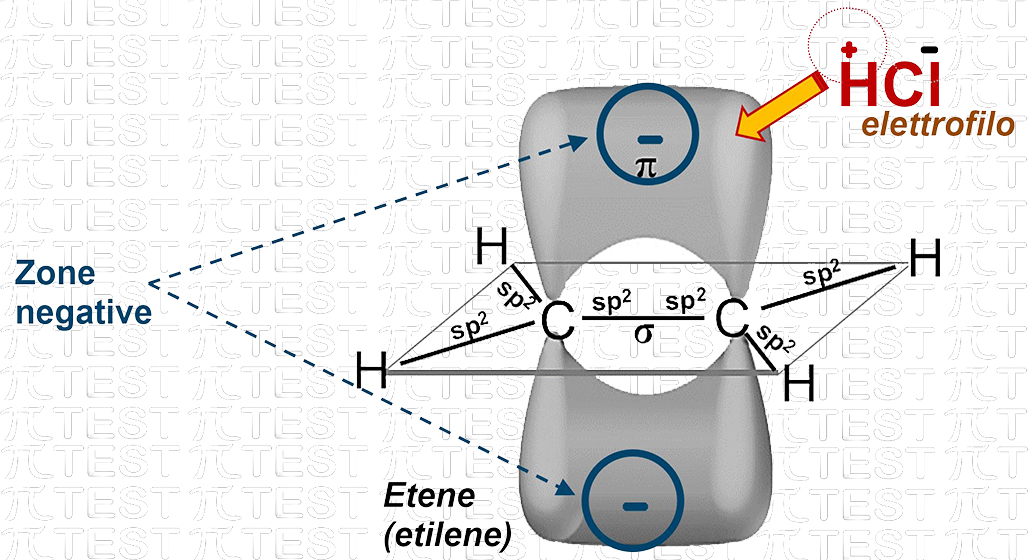
La rottura del secondo legame π porta alla riconfigurazione delle ibridazioni dei due atomi di carbonio interessati. Dall’ibridazione trigonale piana sp2 si passa all’ibridazione tetraedrica sp3. Ciascuno dei due atomi di carbonio ora possiede un legame in più verso l’esterno (avendolo perso come legame interno carbonio-carbonio. L’acido cloridrico HCl rompe il proprio legame interno e avremo che H e Cl separatamente si vanno ad addizionare ai due atomi di carbonio.
La reazione di addizione elettrofila sarà, in sintesi:
CH2=CH2 + HCl → CH3−CH2Cl
La reazione è nota nei passaggi intermedi che comportano la formazione di composti intermedi (carbocatione, ecc.) che non vengono richiesi nei quiz di ammissione.
10.5.2 SOSTITUZIONE ELETTROFILA
La situazione iniziale descritta per l’addizione elettrofila si ripresenta similmente quando un elettrofilo incontra un anello benzenico. L’anello benzenico però è più robusto del legame π e resiste all’attacco. L’effetto finale è quello della sostituzione di un atomo di idrogeno legato al benzene con un altro atomo o un altro gruppo.
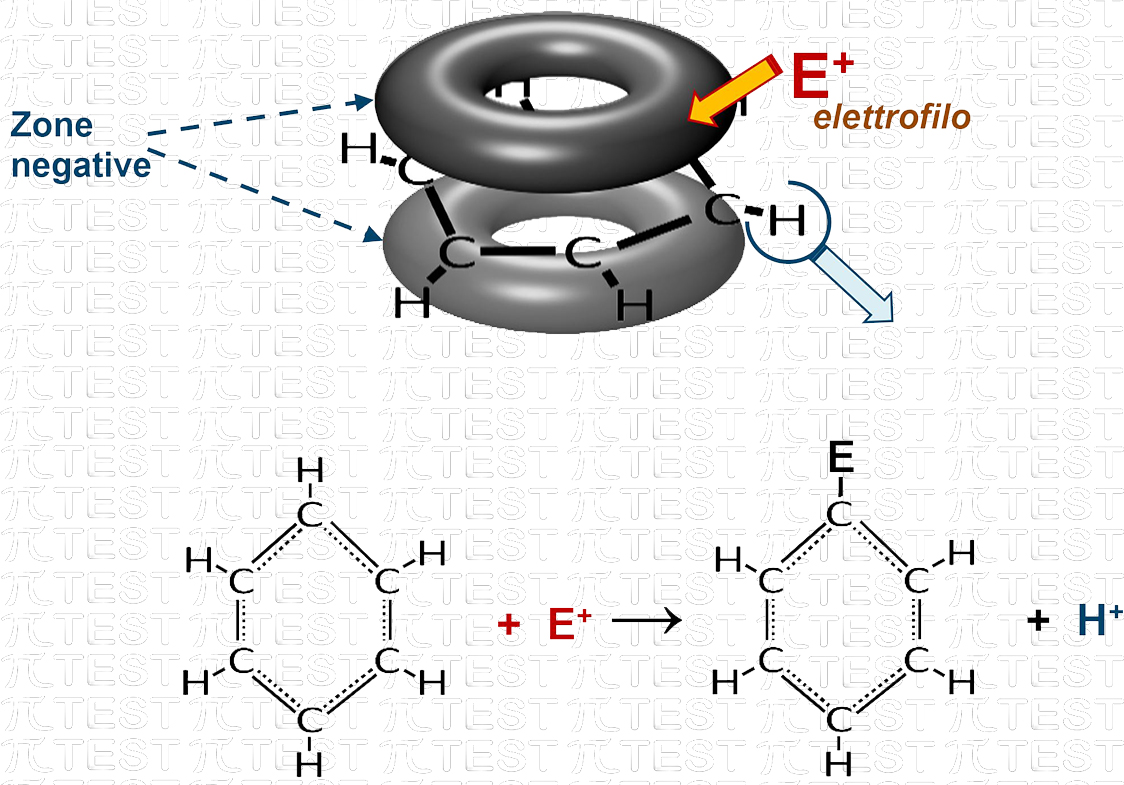
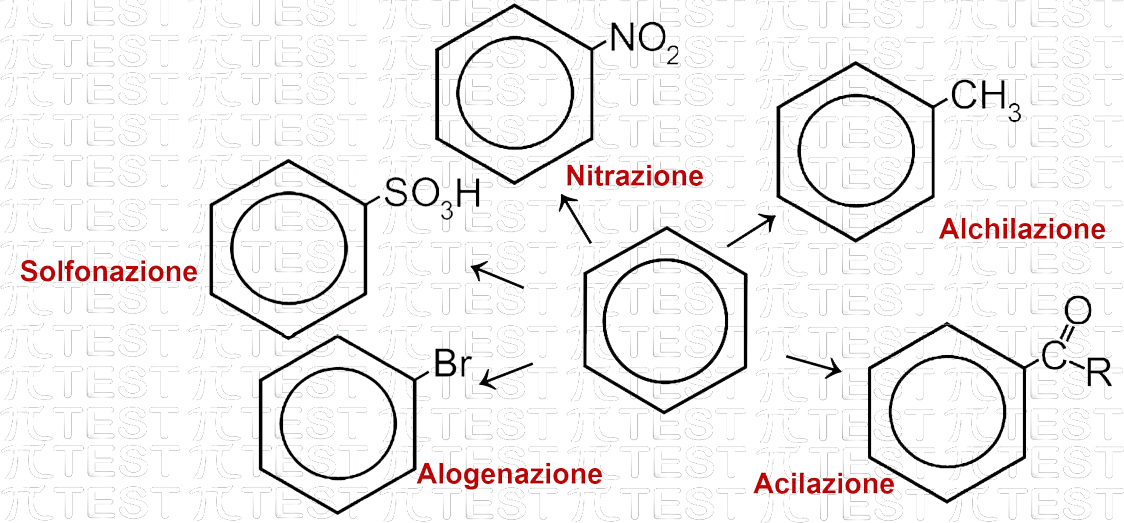
Con questo tipo di reazioni, partendo dal benzene si possono avere per sostituzione moltissimi altri composti.
© il testo è di esclusiva proprietà dell’autore ed è sottoposto a COPYRIGHT – non è consentito alcun utilizzo diverso dallo studio gratuito degli utenti del sito
CONTINUA LO STUDIO DELLA CHIMICA ORGANICA
10.1 Idrocarburi
10.2 Idrocarburi alifatici
10.2.1 Idrocarburi alifatici saturi: gli ALCANI
10.2.2 Radicali alchilici
10.2.3 Idrocarburi ramificati
10.2.4 Proprietà fisiche e chimiche degli alcani
10.2.5 Idrocarburi insaturi: ALCHENI
10.2.6 Proprietà fisiche e chimiche degli alcheni
10.2.7 Idrocarburi insaturi: ALCHINI
10.2.8 Proprietà fisiche e chimiche degli alchini
10.2.9 POLIENI
10.2.10 CICLOALCANI, CICLOALCHENI E COCLOALCHINI
10.2.11 Composti ETEROCICLICI SATURI
10.3 Gli isomeri
10.3.1 Isomeri COSTITUZIONALI DI CATENA
10.3.2 Isomeri COSTITUZIONALI DI POSIZIONE
10.3.3 Isomeri COSTITUZIONALI DI FUNZIONE
10.3.4 Stereoisomeri CONFORMAZIONALI
10.3.5 Stereoisomeri CONFIGURAZIONALI GEOMETRICI
10.3.6 Stereoisomeri CONFIGURAZIONALI OTTICI
10.4 IDROCARBURI AROMATICI
10.4.1 BENZENE
10.4.2 I PRINCIPALI COMPOSTI AROMATICI DERIVANTI DAL BENZENE ‒ ARENI
10.4.3 IDROCARBURI POLICICLICI AROMATICI
10.4.4 COMPOSTI ETEROCICLICI INSATURI
10.5 ADDIZIONE E SOSTITUZIONE ELETTROFILA
10.5.1 ADDIZIONE ELETTROFILA
10.5.2 SOSTITUZIONE ELETTROFILA
10.6 GRUPPI FUNZIONALI
10.6.1 ALOGENURI ALCHILICI E ARILICI
10.6.3 ALCOLI
10.6.4 Proprietà fisiche e chimiche e preparazione degli ALCOL
10.6.5 POLIALCOLI (POLIOLI)
10.6.6 ETERI
10.6.7 CARBONILE – ALDEIDI E CHETONI
10.6.8 CARBOSSILE – ACIDI ORGANICI
10.6.9 ANIDRIDI
10.6.10 ESTERI
10.6.11 LIVELLI DI OSSIDAZIONE DELLE MOLECOLE ORGANICHE
10.6.12 SAPONIFICAZIONE
10.6.13 FOSFOLIPIDI
10.6.14 LIPIDI O GRASSI
10.6.15 AMMINE
10.6.16 AMMIDI
10.6.17 AMMINOACIDI – PROTEINE
10.7 POLIMERI
10.8 CARBOIDRATI


