10.4 IDROCARBURI AROMATICI
In questo raggruppamento troviamo tutti gli idrocarburi che al loro interno contengono uno o più anelli aromatici. Una loro caratteristica è quella di emanare odore.
Si tratta di composti che possiedono una struttura ciclica (ad anello) di atomi di carbonio con la presenza di uno o più doppi legami. Gli elettroni dei secondi legami π si distribuiscono sull’intero anello (sono detti per questo delocalizzati) conferendo alla struttura una buona stabilità.
10.4.1 BENZENE
Il principale anello aromatico è il benzene C6H6.
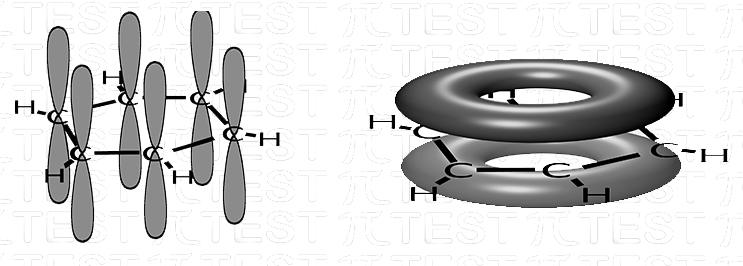
È un anello composto da sei atomi di carbonio disposti in forma perfettamente esagonale su un unico piano. I sei atomi di carbonio sono tutti ibridati sp2 e possiedono tutti un orbitale p (bilobato) che formerà doppi legami.
Il benzene dispone i suoi sei atomi di carbonio sullo stesso piano differentemente dal cicloesano (idrocarburo ciclico saturo con tutti e sei gli atomi di carbonio ibridati sp3) che dispone i sei atomi di carbonio con una conformazione tridimensionale non planare a sedia o a barca.
Come primo approccio alla molecola possiamo immaginare che i doppi legami siano disposti in modo alternato lungo l’anello e che esistano due possibili strutture limite di risonanza.
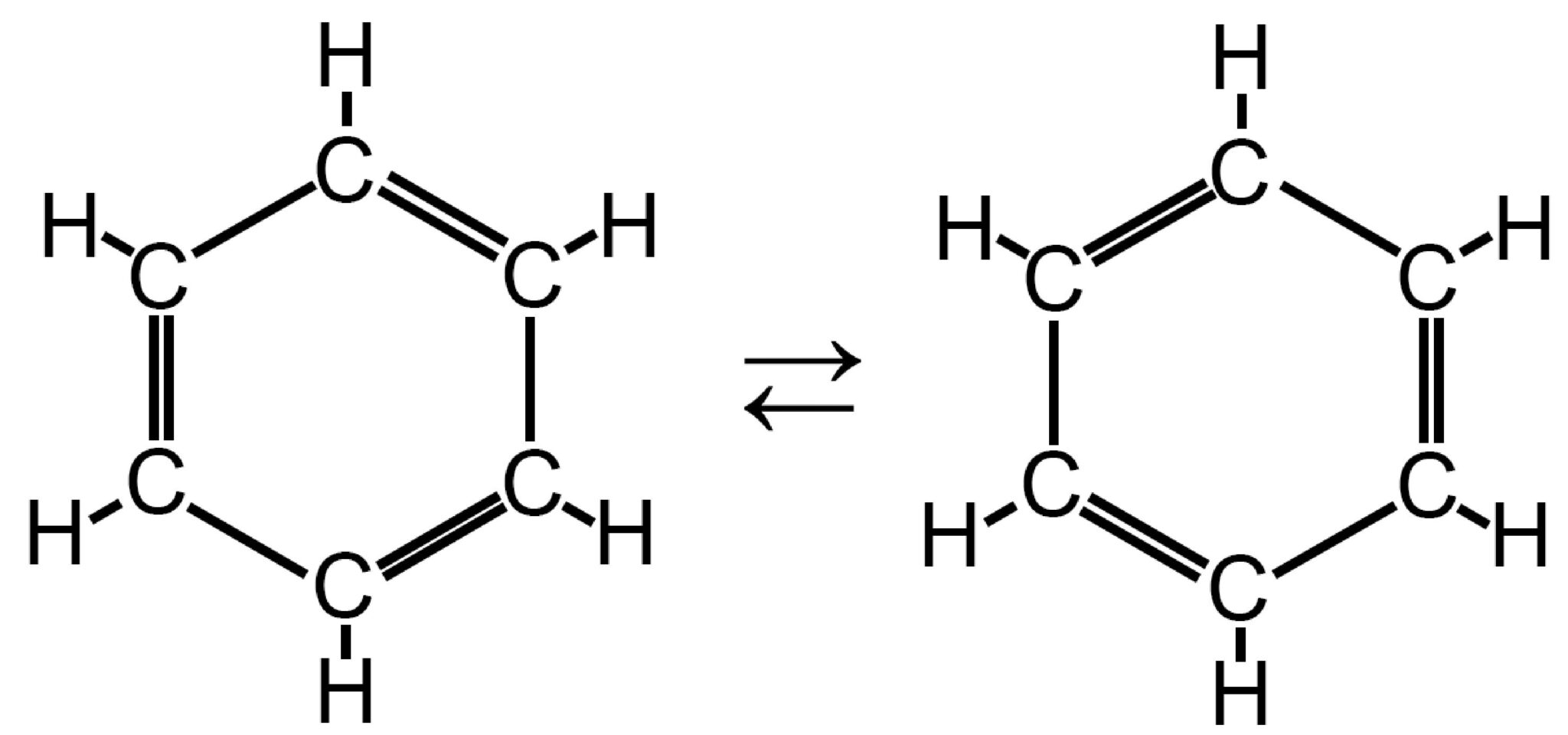
In realtà esiste un’unica forma che fonde di tre secondi legami π in un unico doppio legame con forma di doppio anello; un anello sopra ed un anello sotto così come il legame π è composto da due parti una sopra ed una sotto.
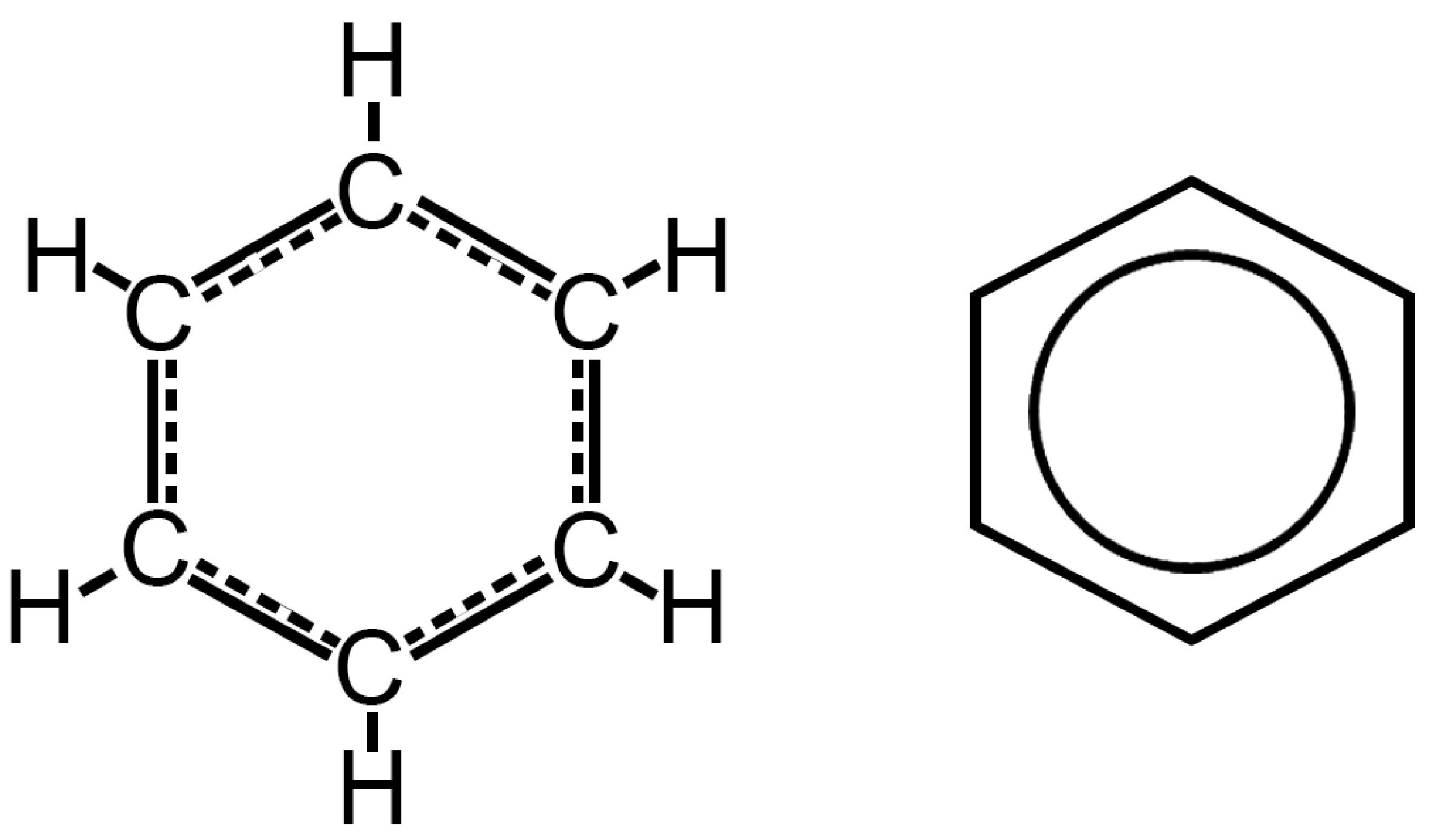
 Per questo motivo si parla spesso di anello del benzene e si raffigura così:
Per questo motivo si parla spesso di anello del benzene e si raffigura così:
10.4.2 I PRINCIPALI COMPOSTI AROMATICI DERIVANTI DAL BENZENE ‒ ARENI
Una grande famiglia di composti derivanti dall’anello benzenico prende il nome di Areni.
Vediamo i più diffusi composti chimici che derivano dal benzene per sostituzione di un atomo di idrogeno con altri gruppi atomici.
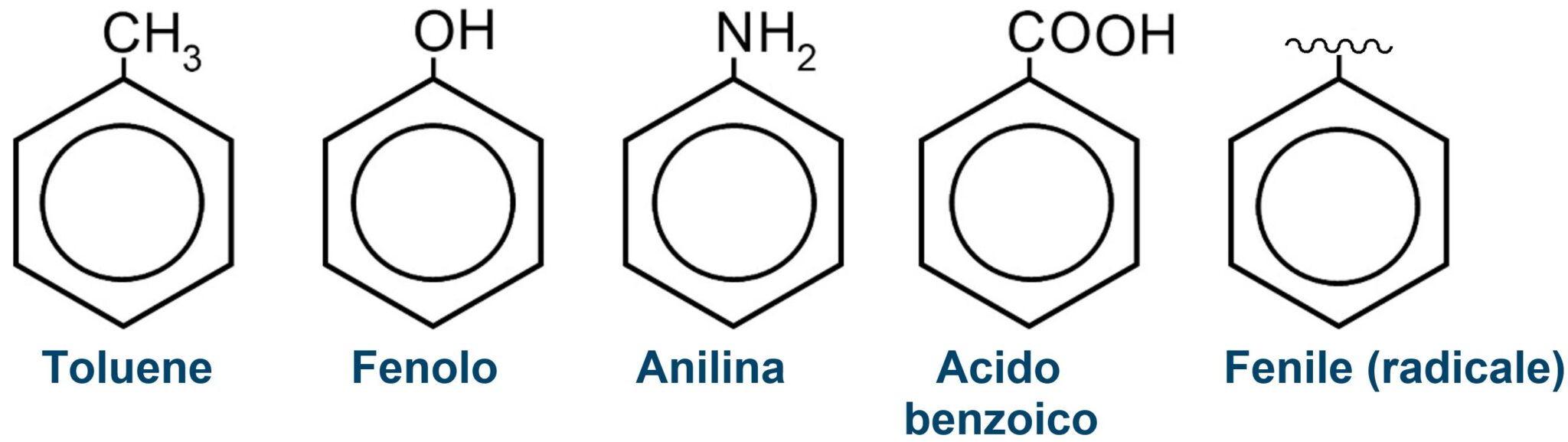 Quando sull’anello del benzene abbiamo due sostituzioni di un atomo di idrogeno con altri gruppi, per indicare le posizioni dei due punti di attacco si usa un sistema di nomenclatura di due diversi tipi.
Quando sull’anello del benzene abbiamo due sostituzioni di un atomo di idrogeno con altri gruppi, per indicare le posizioni dei due punti di attacco si usa un sistema di nomenclatura di due diversi tipi.
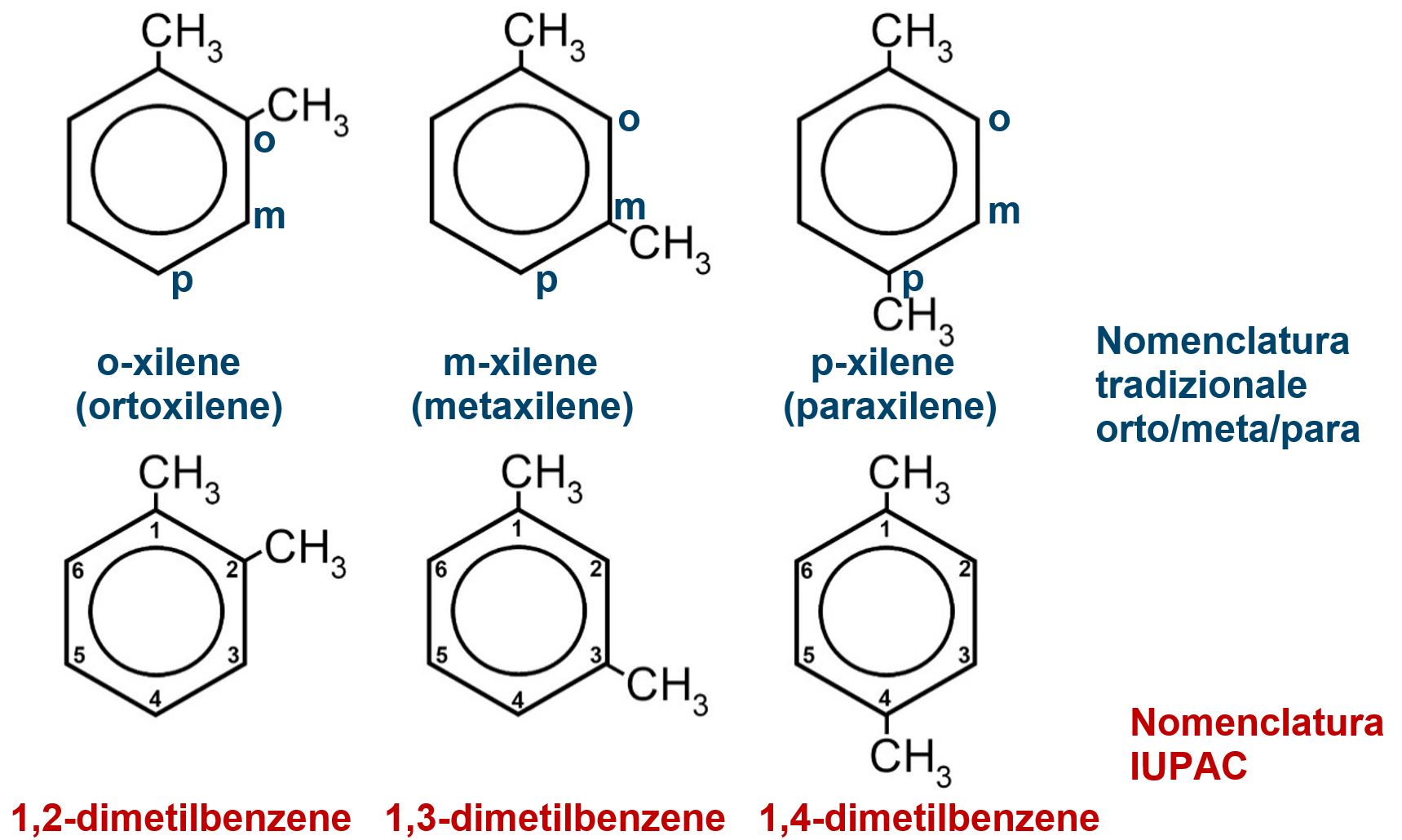
1) Nel sistema tradizionale si utilizza il prefisso orto / meta / para per indicare:
• orto – due posizioni contigue
• meta – per due posizioni con salto di una posizione
• para – per due posizioni opposte
2) Nella nomenclatura IUPAC si indicano con numeri a 1 a 6 i sei atomi di carbonio del benzene; con tale numerazione la nomenclatura indica con due numeri i due atomi di carbonio che vedono la sostituzione dell’atomo di idrogeno con altri gruppi.
Come esempio consideriamo lo xilene, un composto basato sul benzene con due gruppi metilici che sostituiscono due atomi di idrogeno.
Quando un anello benzenico è collegato ad una catena alifatica il nome del radicale prende il nome di Fenile:
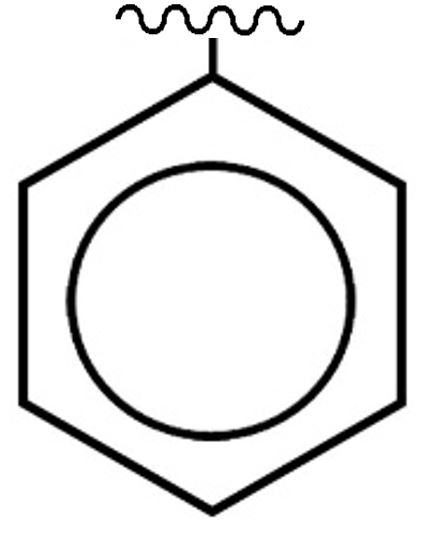 |
Fenile −C6H5
gruppo funzionale che deriva dal benzene dovuto alla perdita di un atomo di idrogeno |
Più in generale utilizziamo il termine di RADICALE ARILICO per indicale un idrocarburo aromatico che presenta un legame possibile verso altre strutture chimiche al posto di un suo atomo di idrogeno.
10.4.3 IDROCARBURI POLICICLICI AROMATICI
Possiamo trovare in natura composti contenenti più anelli aromatici connessi tra loro. I più noti sono i seguenti.
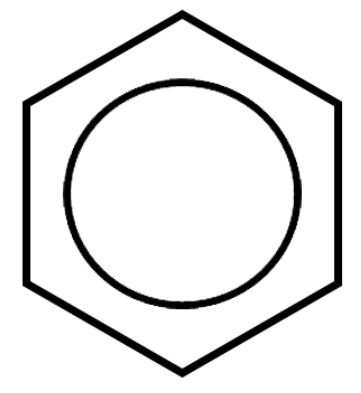 |
Benzene C6H6 |
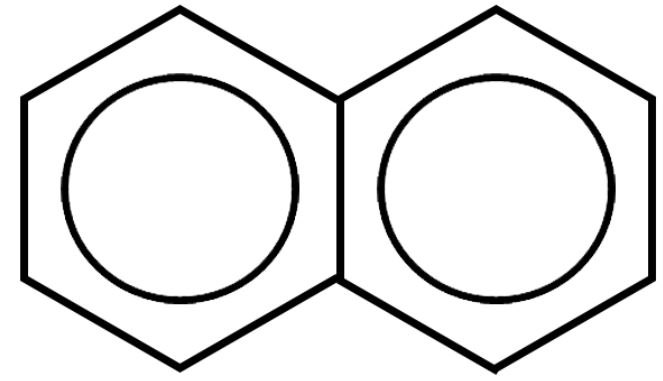 |
Naftalene C10H8 |
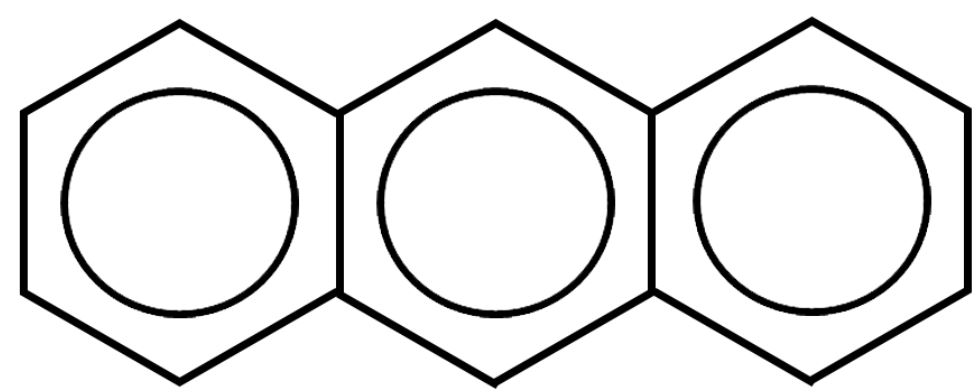 |
Antracene C14H10 |
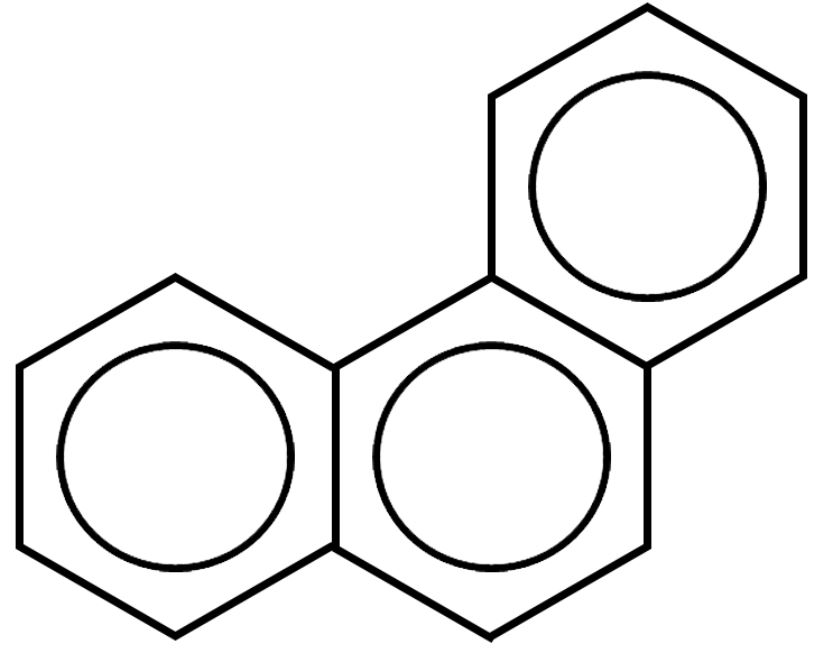 |
Fenantrene C14H10 |
10.4.4 COMPOSTI ETEROCICLICI INSATURI
Così come per i composti cicli saturi (vedi), abbiamo numerosissimi composti ciclici insaturi con un atomo di carbonio sostituito da un altro elemento, per lo più ossigeno, azoto e zolfo. Ne citiamo solo alcuni, in quanto un approfondimento sistematico dei diversi composti eterociclici insaturi sarebbe inutile per lo studio che è finalizzato al superamento dei test di ammissione all’università. Nello studio dell’esame universitario di chimica organica lo studente avrà modo di approfondire ulteriormente.
Il PIRROLO è importante perché quattro anelli pirrolici tra di loro collegati costituiscono il gruppo eme presente nell’emoglobina ed anche la clorofilla.
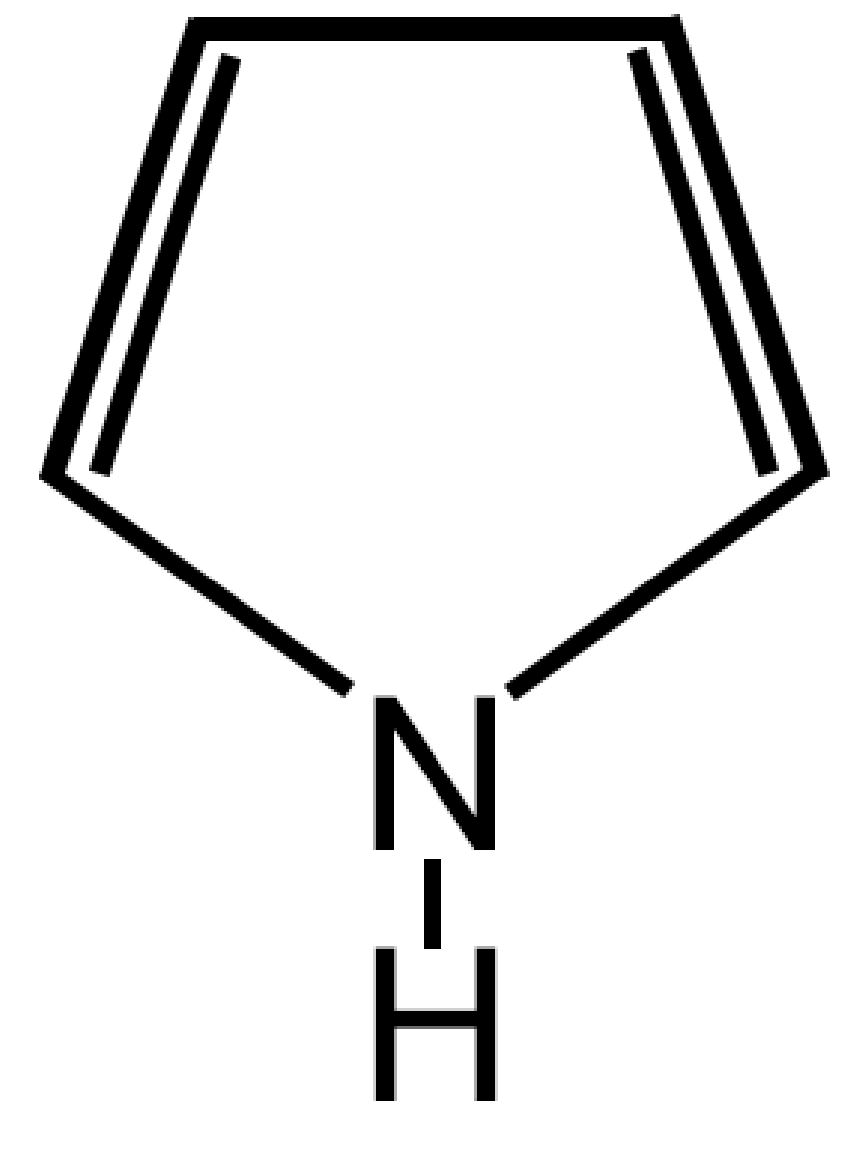 |
Pirrolo C4H5N |
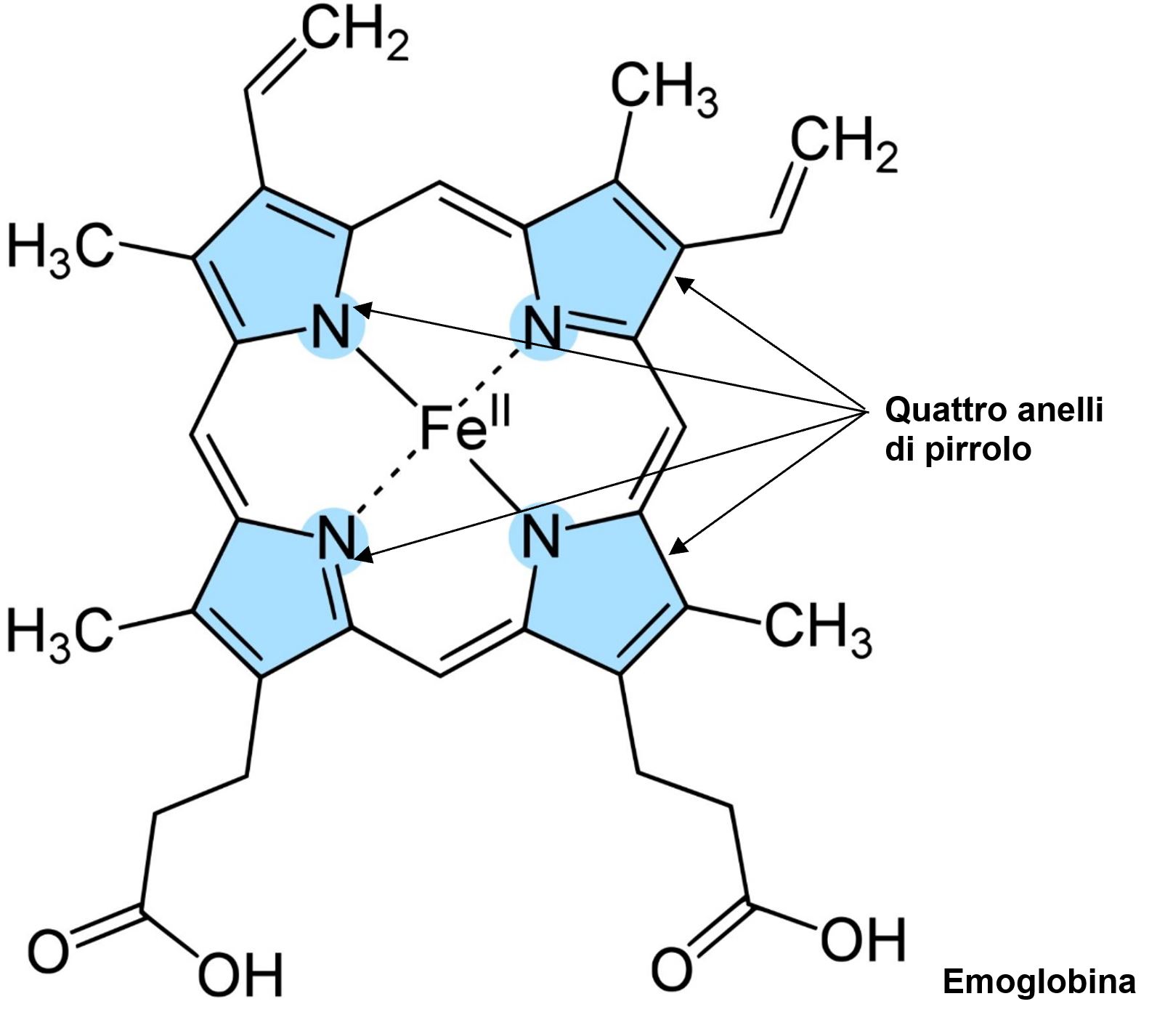
È bene puntualizzare che un composto aromatico si può basare sia su una struttura esagonale (benzene), su una struttura pentagonale e su strutture policicliche.
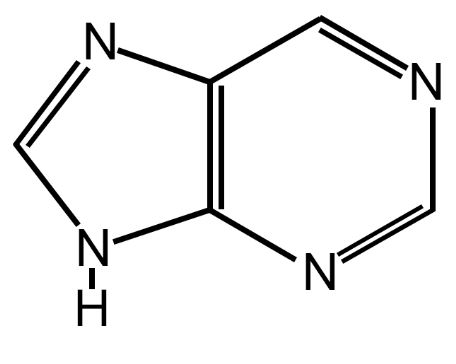
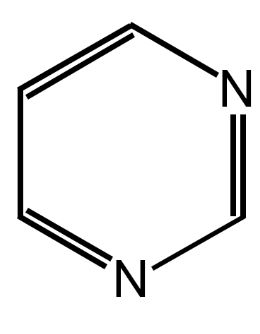
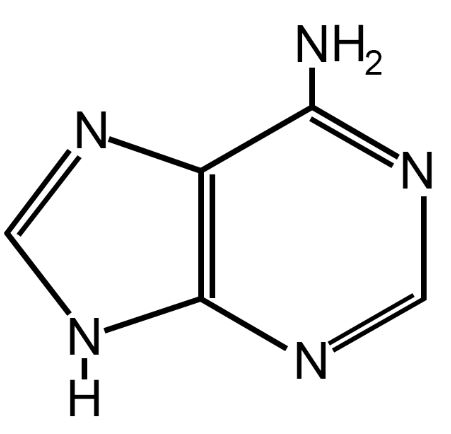
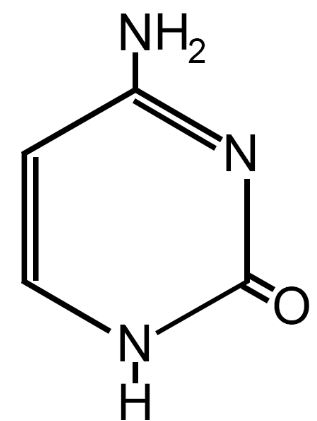
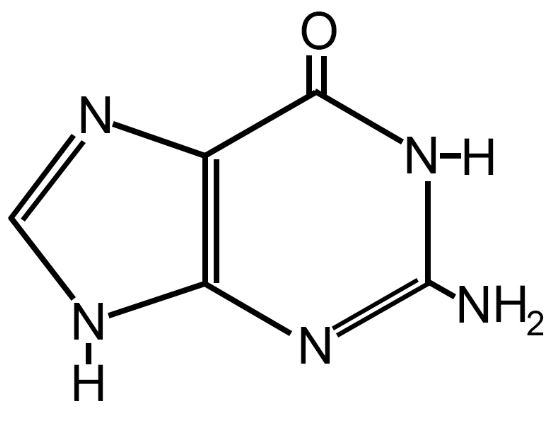
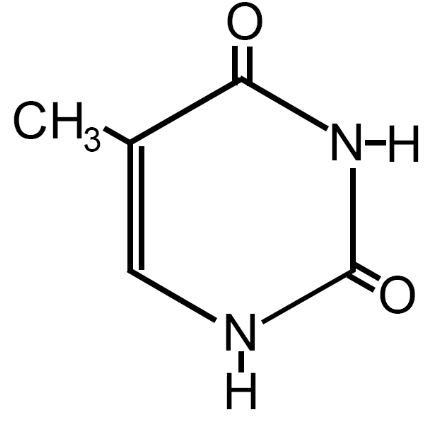
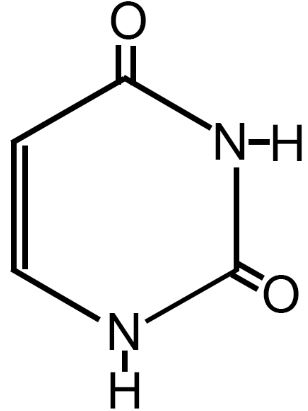
Tra queste abbiamo le cinque basi azotate del DNA e dell’RNA; le due purine (adenina e guanina) e le tre pirimidine (citosina, timina e uracile).
© il testo è di esclusiva proprietà dell’autore ed è sottoposto a COPYRIGHT – non è consentito alcun utilizzo diverso dallo studio gratuito degli utenti del sito
CONTINUA LO STUDIO DELLA CHIMICA ORGANICA
10.1 Idrocarburi
10.2 Idrocarburi alifatici
10.2.1 Idrocarburi alifatici saturi: gli ALCANI
10.2.2 Radicali alchilici
10.2.3 Idrocarburi ramificati
10.2.4 Proprietà fisiche e chimiche degli alcani
10.2.5 Idrocarburi insaturi: ALCHENI
10.2.6 Proprietà fisiche e chimiche degli alcheni
10.2.7 Idrocarburi insaturi: ALCHINI
10.2.8 Proprietà fisiche e chimiche degli alchini
10.2.9 POLIENI
10.2.10 CICLOALCANI, CICLOALCHENI E COCLOALCHINI
10.2.11 Composti ETEROCICLICI SATURI
10.3 Gli isomeri
10.3.1 Isomeri COSTITUZIONALI DI CATENA
10.3.2 Isomeri COSTITUZIONALI DI POSIZIONE
10.3.3 Isomeri COSTITUZIONALI DI FUNZIONE
10.3.4 Stereoisomeri CONFORMAZIONALI
10.3.5 Stereoisomeri CONFIGURAZIONALI GEOMETRICI
10.3.6 Stereoisomeri CONFIGURAZIONALI OTTICI
10.4 IDROCARBURI AROMATICI
10.4.1 BENZENE
10.4.2 I PRINCIPALI COMPOSTI AROMATICI DERIVANTI DAL BENZENE ‒ ARENI
10.4.3 IDROCARBURI POLICICLICI AROMATICI
10.4.4 COMPOSTI ETEROCICLICI INSATURI
10.5 ADDIZIONE E SOSTITUZIONE ELETTROFILA
10.5.1 ADDIZIONE ELETTROFILA
10.5.2 SOSTITUZIONE ELETTROFILA
10.6 GRUPPI FUNZIONALI
10.6.1 ALOGENURI ALCHILICI E ARILICI
10.6.3 ALCOLI
10.6.4 Proprietà fisiche e chimiche e preparazione degli ALCOL
10.6.5 POLIALCOLI (POLIOLI)
10.6.6 ETERI
10.6.7 CARBONILE – ALDEIDI E CHETONI
10.6.8 CARBOSSILE – ACIDI ORGANICI
10.6.9 ANIDRIDI
10.6.10 ESTERI
10.6.11 LIVELLI DI OSSIDAZIONE DELLE MOLECOLE ORGANICHE
10.6.12 SAPONIFICAZIONE
10.6.13 FOSFOLIPIDI
10.6.14 LIPIDI O GRASSI
10.6.15 AMMINE
10.6.16 AMMIDI
10.6.17 AMMINOACIDI – PROTEINE
10.7 POLIMERI
10.8 CARBOIDRATI