TEST DI AMMISSIONE A MEDICINA ED ODONTOIATRIA
Anno Accademico 2022/2023
Quiz n°10 – Biologia
Medicina 2022
Gli esempi di seguito riportati sono determinati da interazioni deboli ECCETTO UNO, quale?
Ricordiamo la distinzione tra legami molecolari - forti (legami covalenti e strutture ioniche cristalline) e legami intermolecolari - deboli (di Van der Waals, dipolo-dipolo e a ponte idrogeno).
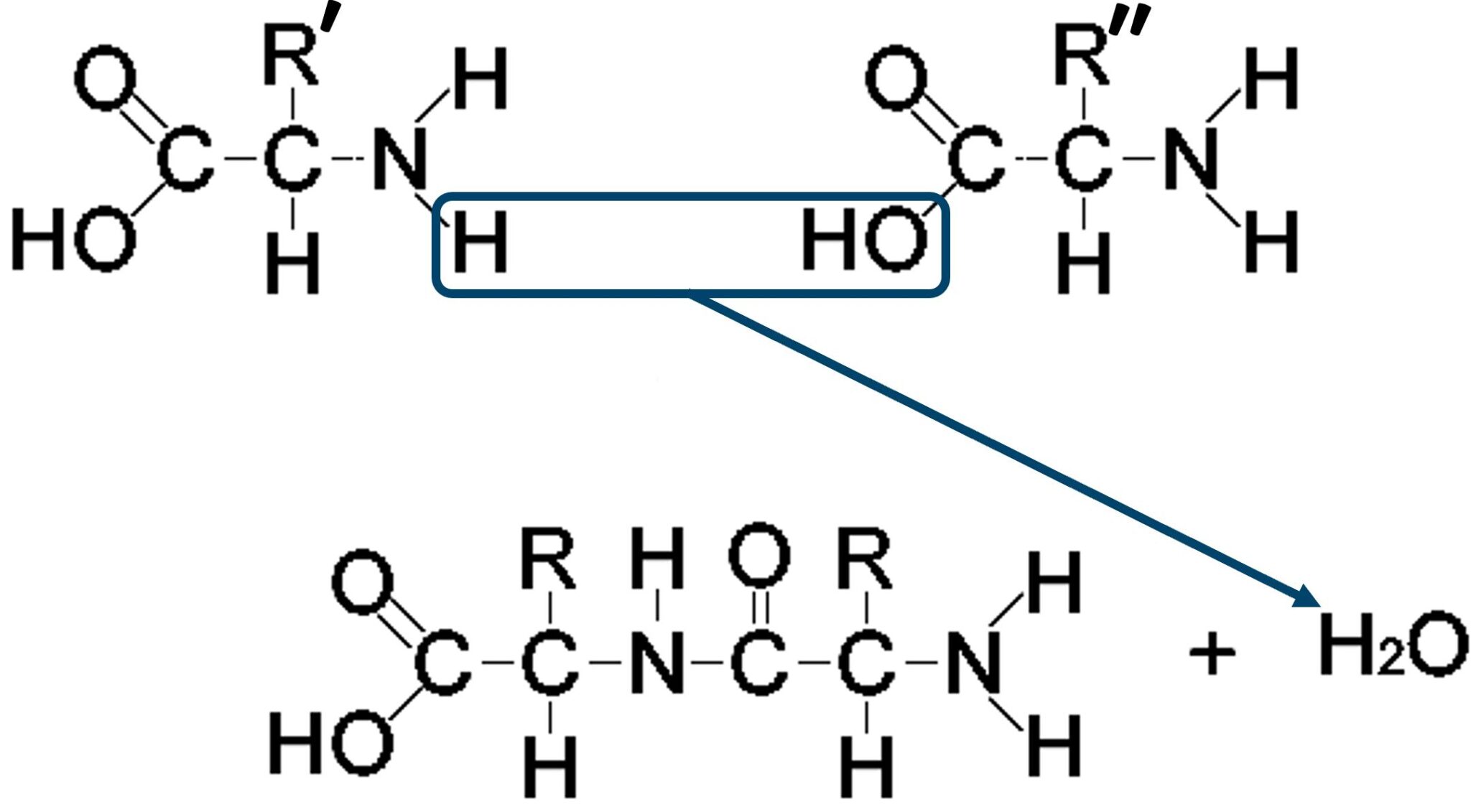
La struttura primaria delle proteine (risp. D) è data da una sequenza di amminoacidi legati da legami peptidici, tipicamente covalenti. Il legame peptidico si forma con una reazione di condensazione tra il gruppo funzionale carbossilico -COOH e il gruppo funzionale amminico -NH2 con eliminazione di una molecola di acqua. Il carbonio del carbossile di un primo amminoacido si ritrova legato con legame covalente all'azoto del gruppo amminico del secondo amminoacido.
Gli altri legami sono interazioni deboli in quanto si tratta di legami intermolecolari. L'appaiamento Codone-anticodone avviene per ponti idrogeno.
Il legame intermolecolare che si forma tra l'antigene e l'anticorpo può essere ionico, legato alle forze di Van der Waals o a ponti idrogeno; tutti legami intermolecolari (legami deboli).
La struttura secondaria delle proteine caratterizza la disposizione spaziale della proteina nelle forme α-elica o β-foglietto e dovuta a legami a pronte idrogeno.
Le acquaporine costituiscono i canali proteici che permettono all'acqua di attraversare le membrane cellulari; esse interagiscono con l'acqua per quel poco che serve a permettere all'acqua di spostarsi.
Test di Medicina 2022 - Quiz |
|||
|---|---|---|---|


