p.san 2004
Nella titolazione tra HCl ed NaOH il punto di equivalenza si raggiunge a :
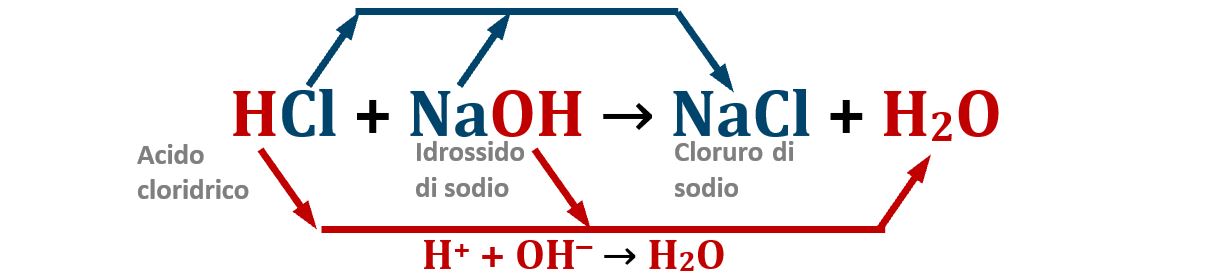
Una titolazione può essere vista come un neutralizzazione aggiungendo un acido ad una soluzione basica o viceversa. Se si neutralizza un acido forte con una base forte (come nel caso esposto nel quiz nel qual e abbiamo HCl-acido forte e NaOH-base forte), il punto di equivalenza si ottiene quando il numero di moli dell'acido sono uguali al numero di moli della base. gli ioni ossidrile OH– si neutralizzano tutti con gli ioni H+ e la soluzione finale conterrà cloruro di sodio e sarà neutra, come afferma la risposta E).
Diversamente accade se si neutralizza una base debole come ad esempio NH3 con un acido forte come HCl, perché al punto di equivalenza avremo il sale cloruro di ammonio che è un sale acido ed il pH sarà inferiore a 7. Discorso analogo sarebbe se neutralizziamo un acido debole come l'acido acetico CH3COOH con una base forte come NaOH, perché avremmo il sale acetato di sodio che è un sale basico ed il pH sarà superiore a 7.


