Prof.san 2005
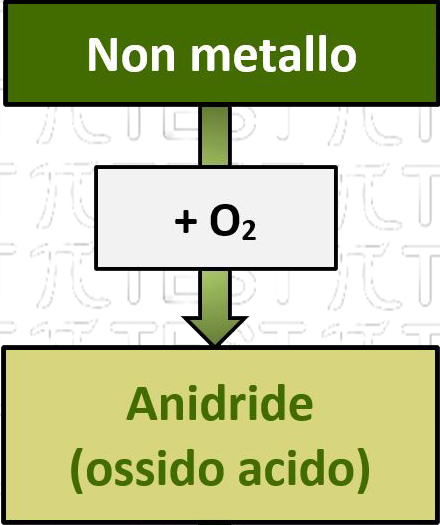
La reazione tra un non metallo e l'ossigeno forma:
Un non metallo reagisce con l’ossigeno formando un composto binario, l’anidride (detto anche ossido acido perché da questa in future reazioni si formeranno composti acidi) la cui formula chimica dipende dal numero di ossidazione del non metallo.
I non metalli possono avere una serie di numeri di ossidazione più ampia e per le desinenze da utilizzare nella nomenclatura non bastano le due desinenze –osa e –ica ma si adottano anche prefissi secondo il seguente schema:

Lo zolfo S posside i numeri di ossidazione +4 e +6. Sormerà così l’anidride solforosa e l’anidride solforica

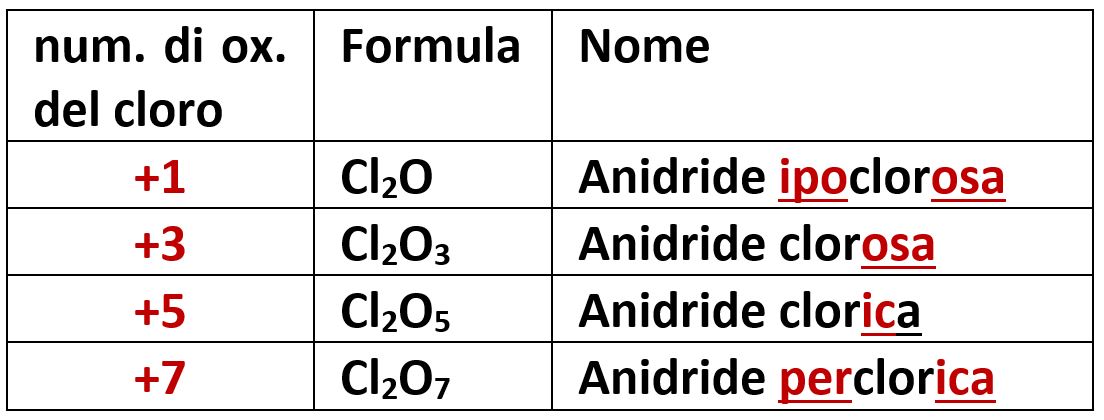
Gli alogeni possiedono tutti il numero di ossidazione -1 (che vedremo tra poco nella formazione degli idracidi) e alcuni tra i valori +1, +3, +5, +7. Tra gli alogeni solo il cloro Cl possiede tutti questi valori ed avremo quattro diverse anidridi.
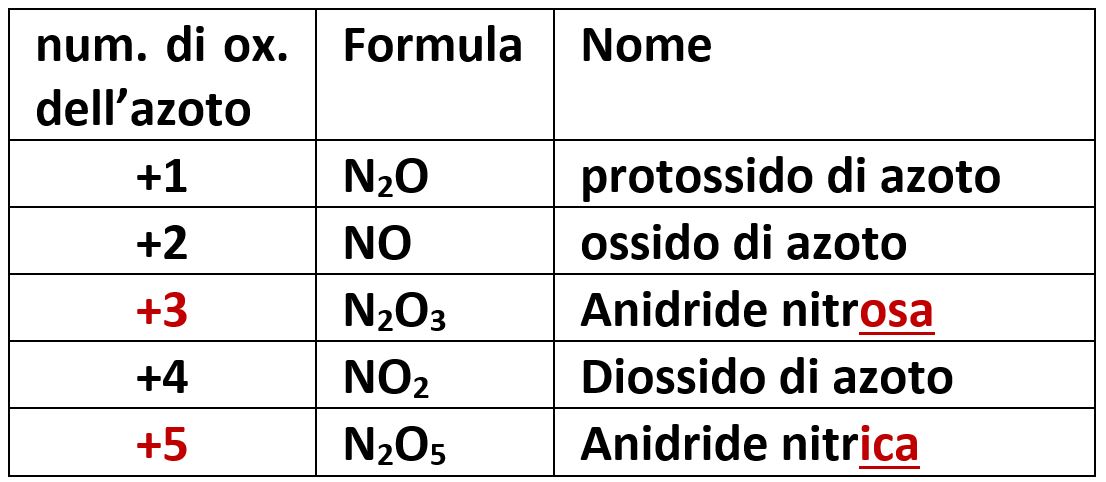
L’azoto N possiede i numeri di ossidazione +1, +2, +3, +4, +5 e con l’ossigeno diversi ossidi. Con i valori +3 e +5 forma N2O3 e N2O5 che chiamiamo anidride nitrosa e anidride nitrica, con gli altri valori forma altri tipi di ossidi.