9.12 Sali neutri, acidi e basici
QUIZ 09
Medicina 2005
Quando si scioglie in acqua il bicarbonato di sodio (NaHCO3) si forma una soluzione:
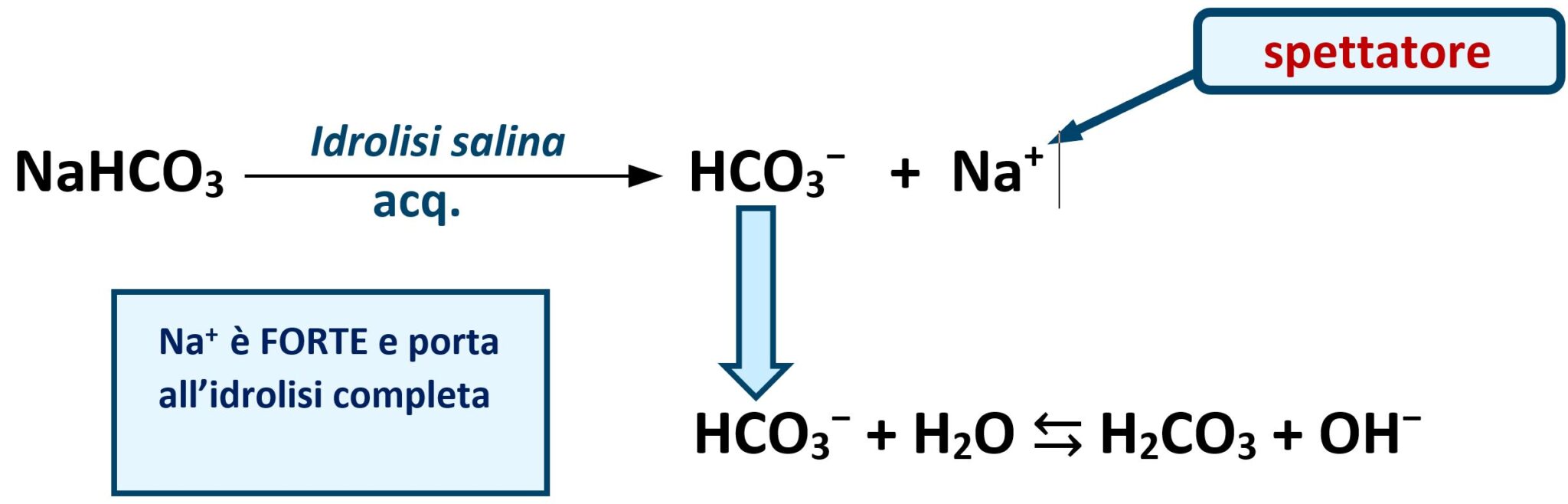
Il bicarbonato di sodio NaHCO3 è un sale del tipo Forte-Debole. Deriva infatti dalla combinazione della base Forte idrossido di sodio NaOH che conferisce al sale il catione Na+ e dell'acido Debole acido carbonico H2CO3 che conferisce al sale l'anione bicarbonato HCO3–. Quando il bicarbonato di sodio viene immesso in acqua, il catione Na+ derivando da una base forte provoca l'idrolisi completa del sale; ha un comportamento neutro ed è detto ione spettatore. Si ritrova così in soluzione l'anione bicarbonato HCO3– che è la base coniugata dell'acido debole acido carbonico. La natura basica dell'anione bicarbonato porta alla reazione che libera ioni ossidrile OH– in acqua rendendola basica:
HCO3– + H2O → H2CO3 + OH–
© il testo è di esclusiva proprietà dell’autore ed è sottoposto a COPYRIGHT – non è consentito alcun utilizzo diverso dallo studio gratuito degli utenti del sito


