Medicina 2004
Quando si scioglie in acqua un sale che si può considerare derivato da un acido forte e da una base forte, la soluzione che si ottiene ha pH neutro. I sali formati da basi forti ed acidi deboli danno luogo a soluzioni basiche, mentre i sali formati da acidi forti e basi deboli danno luogo a soluzioni acide. Una certa soluzione di cloruro di ammonio ha pH = 6,2; una certa soluzione di cianuro di cesio ha pH = 8,4. Pertanto si può affermare che:
Il testo del quiz espone in modo succinto il comportamento dei sali in acqua (vedi la teoria).
Il cloruro di ammonio NH4Cl in acqua porta ad un pH acido (pH 6,2). Ha origine dalla neutralizzazione di un acido forte HCl con una base debole NH3. Lo ione “spettatore” di origine forte Cl‒ non reagisce in acqua e per la sua natura forte in acqua rimane in forma ionica. Di conseguenza alla natura indipendente di Cl‒ , anche lo ione ammonio è costretto a stare in acqua in forma ionica; lo ione ammonio, per la sua natura debole, tende a riformare la base ammoniaca:
NH4+ + H2O ⇆ NH3 + H3O+
così facendo si libera in acqua uno ione H+ determinando una certa acidità della soluzione. In sintesi cloruro di ammonio NH4Cl in acqua possiede un comportamento acido.
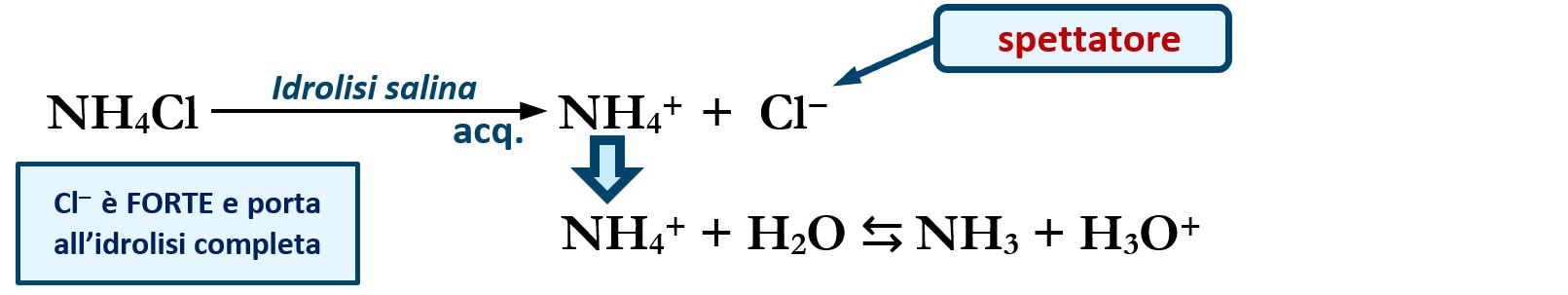
Così esposta la natura del sale cloruro di ammonio è evidente. Il quiz chiede di dedurre dalle informazioni date che l'ammoniaca, base coniugata dello ione ammonio, è appunto una base. Un ragionamento deduttivo come sembrerebbe richiesto dal test non è immediato, ma si può arrivare alla soluzione conoscendo la natura del sale.
Ragionamento analogo si può fare per l'altro sale, il cianuro di cesio CsCN, meno noto agli studenti, che in acqua porta ad una soluzione basica (pH 8,4).
Il cesio Cs è un metallo alcalino (primo gruppo) il cui unico possibile ione è Cs+ di natura forte, come tutti gli ioni degli elementi dei primi due gruppi della tavola periodica degli elementi.
Lo ione cianuro CN– è la forma ionica del gruppo ciano C≡N. deriva dall'acido cianidrico HCN, acido debole. Lo ione cianuro è così la base coniugata dell'acido cianidrico.
Il nostro sale risulta così costituito dal catione spettatore Cs+ e dall'anione cianuro CN–, base debole coniugata dell'acido debole acido cianidrico. Proprio lo ione cianuro, base debole, conferisce al sale la natura basica


