4.5 Ibridazione degli orbitali
QUIZ 10
Veterinaria 2015
La tabella sottostante mostra a quale gruppo della Tavola Periodica appartengono i singoli elementi:
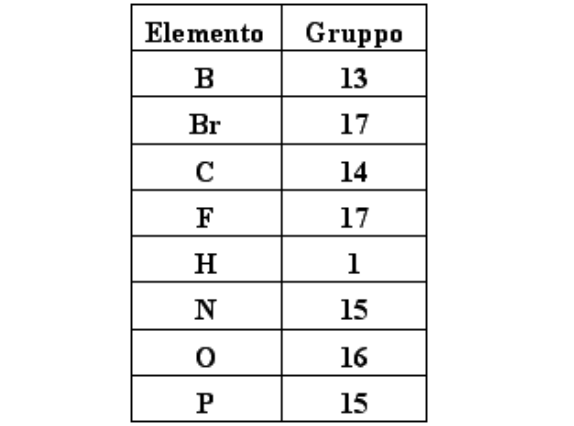 Quale delle seguenti molecole o ioni ha la stessa forma della fosfina (PH3)?
Quale delle seguenti molecole o ioni ha la stessa forma della fosfina (PH3)?
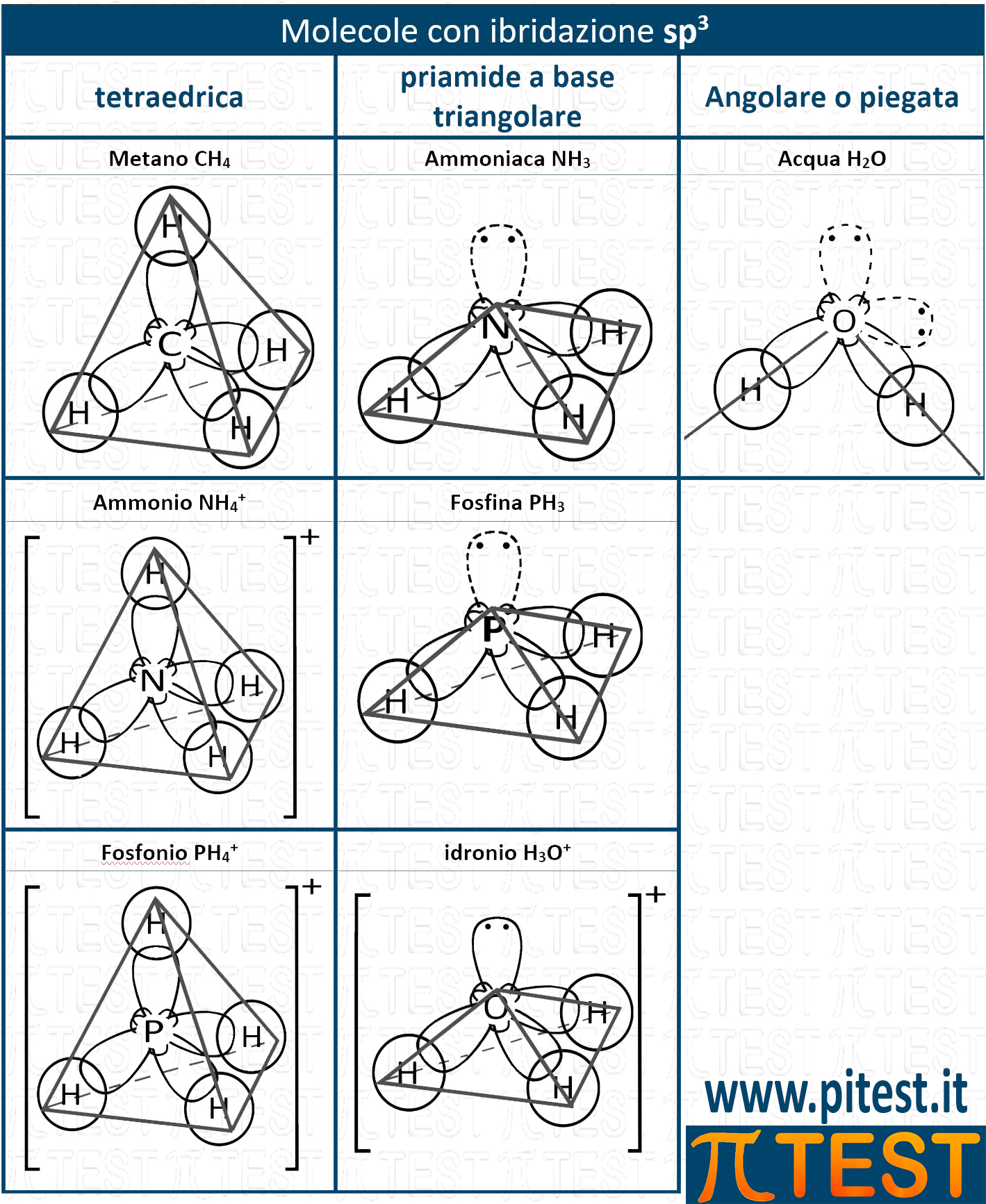
È importante conoscere bene le ibridazioni degli orbitali. Vedi la teoria.
Nella tavola periodica il fosforo appartiene allo stesso gruppo dell’azoto (gruppo 15) e per questo motivo ha un comportamento simile. Forma così un composto del tutto analogo all’ammoniaca, la fosfina che possiede caratteristiche simili.
| Il fosforo P, come l’azoto N, può avere una ibridazione sp3. Con la configurazione elettronica 1s22s22p63s23p3 può formare una ibridazione degli orbitali 3s e 3p formando sp3. Come accade per l’azoto, uno dei quattro orbitali sp3 possiede due elettroni e non formerà legami covalenti classici come gli altri tre. | 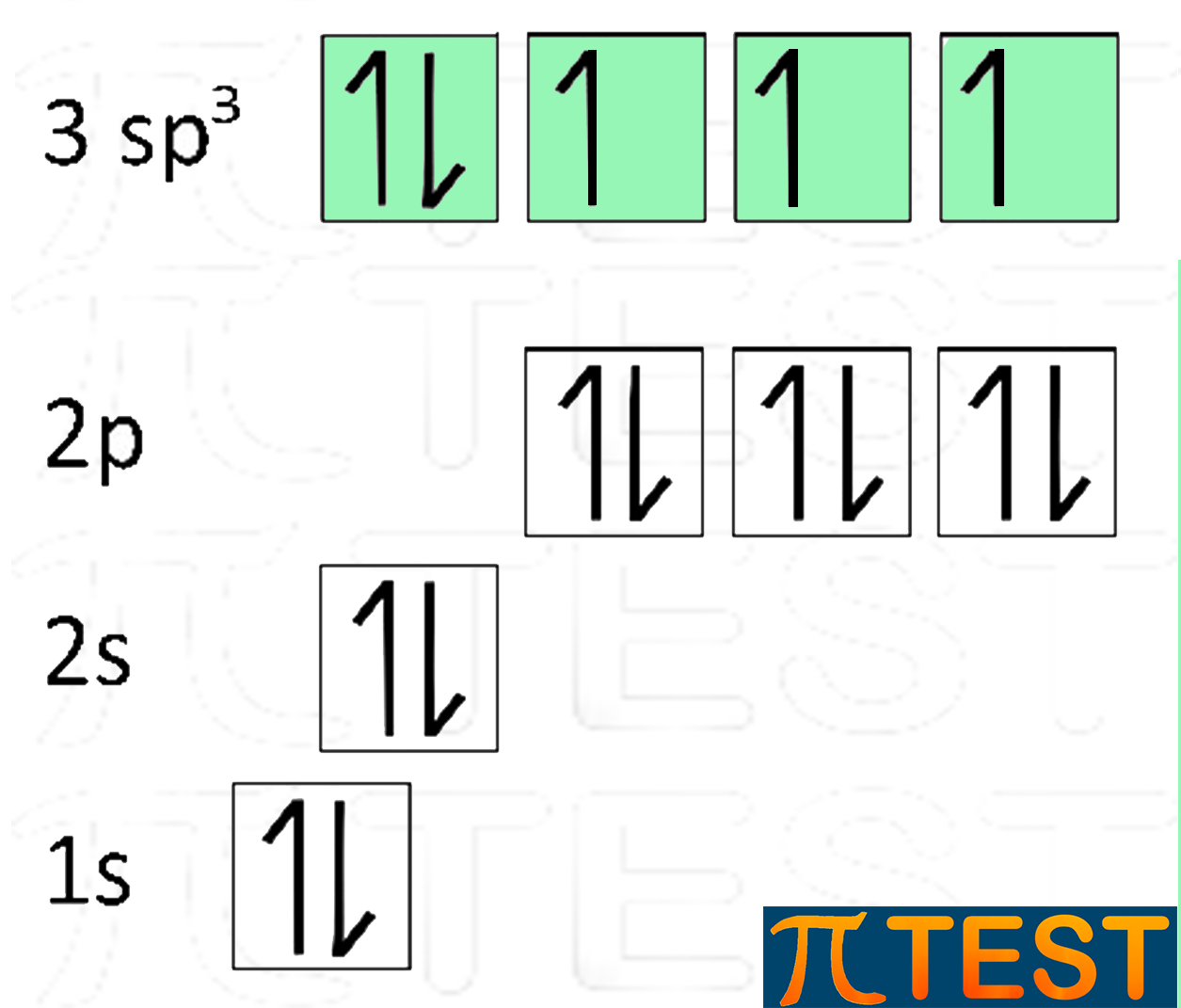 |
|
La molecola che tipicamente si utilizza per esemplificare l’ibridazione sp3 del fosforo è quella della fosfina PH3. 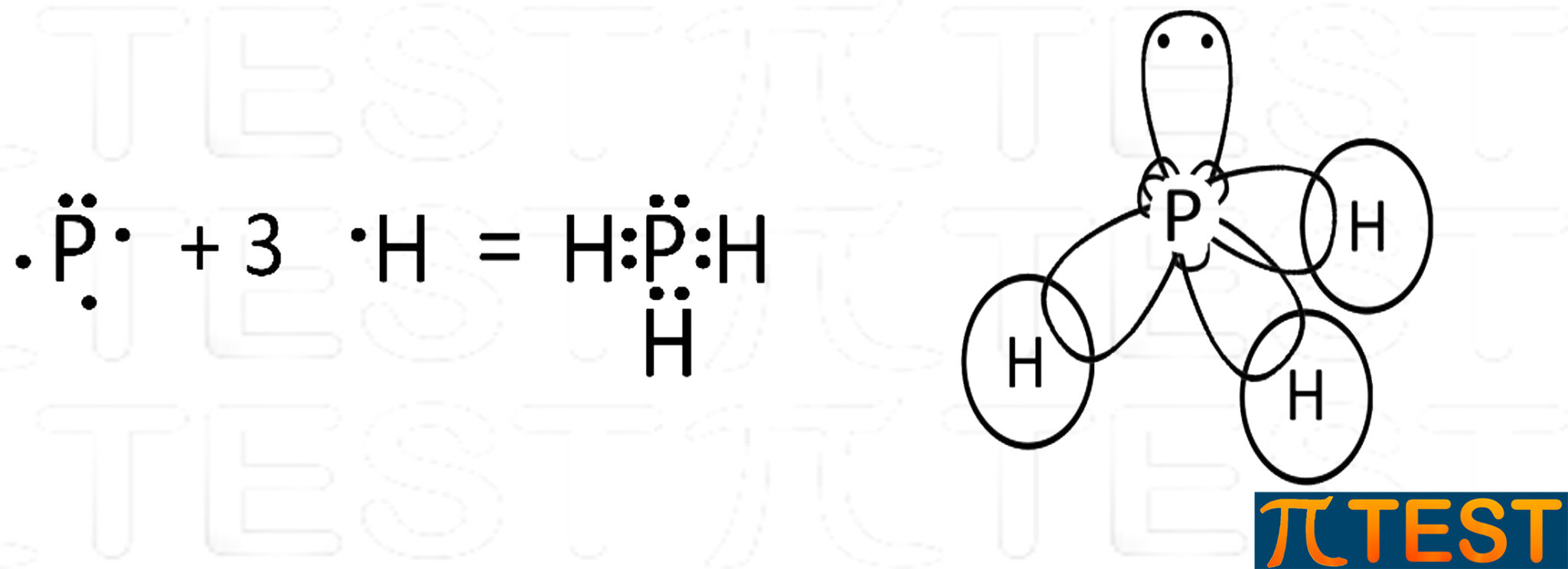 |
|
| Nel considerare la forma complessiva della molecola di fosfina non si considera l’ingombro del doppietto libero, ma solo gli ingombri dovuti ai singoli atomi. Coì come per l’ammoniaca, possiamo dire così che la forma è quella di una piramide a base triangolare (non regolare però come il tetraedro del metano). | 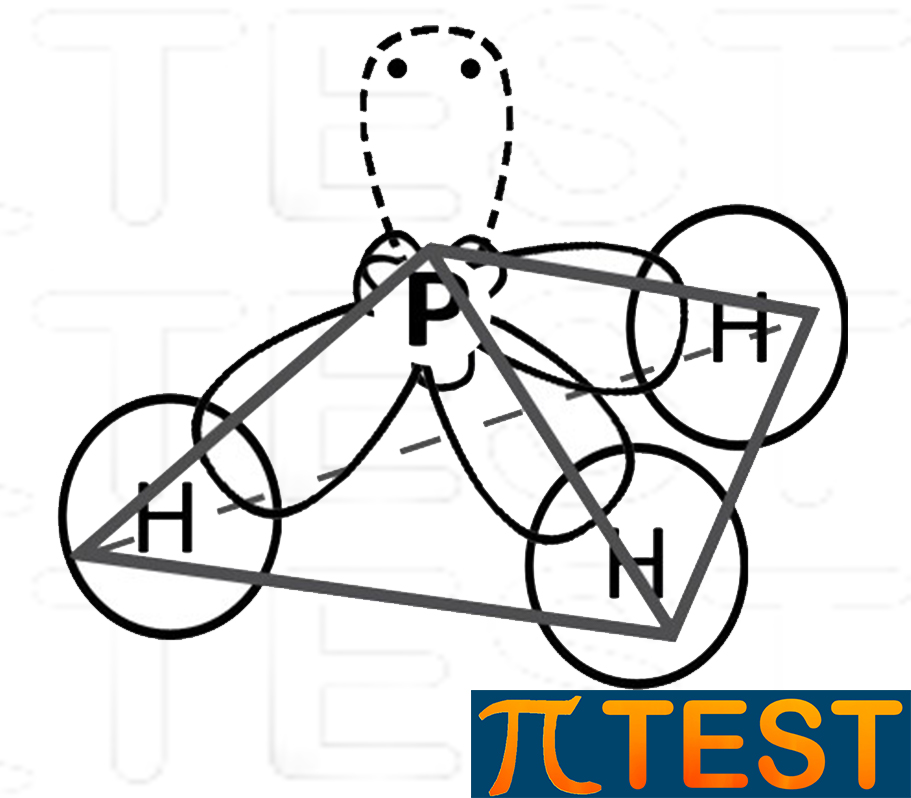 |
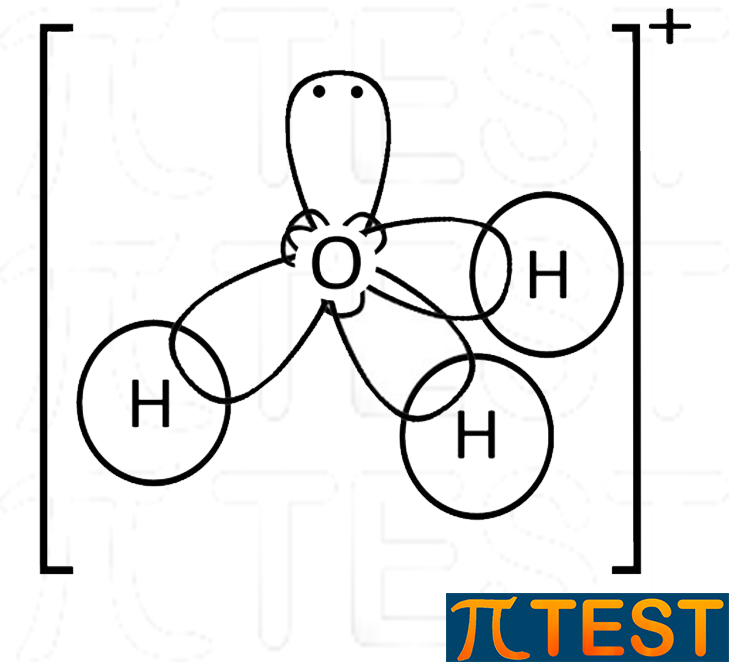
La molecola che possiede la stessa struttura piramidale è quella dell'idronio H3O+.
| Idronio H3O+
l’acqua può formare un terzo legame dativo con H+ andando a formare il catione idronio: H2O + H+ = H3O+ L’idronio H3O+ ha la forma a piramide a base triangolare identica a quella dell’ammoniaca e della fosfina, l’unica differenza consiste nella carica elettrica complessiva +1. |
 |
QUIZ Ibridazione degli orbitali |
|||
|---|---|---|---|
© il testo è di esclusiva proprietà dell’autore ed è sottoposto a COPYRIGHT – non è consentito alcun utilizzo diverso dallo studio gratuito degli utenti del sito


