Veterinaria 2010
Quanti ml di acqua devono essere aggiunti a 150 ml di una soluzione 0,4 M per avere una concentrazione finale pari a 0,1 M?
Per le diluizioni utilizziamo la formula (*):
M1 · V1 = M2 · V2
dove M1 e M2 rappresentano le concentrazioni molari rispettive delle soluzioni iniziale e finale, e V1 and V2 rappresentano i loro volumi. Possiamo interpretare questa formula dicendo che Volume e Molarità sono tra loro inversamente proporzionali. Da questa formula possiamo ricavare qualsiasi grandezza incognita delle quattro. Per il presente quiz ricaviamo il volume finale:
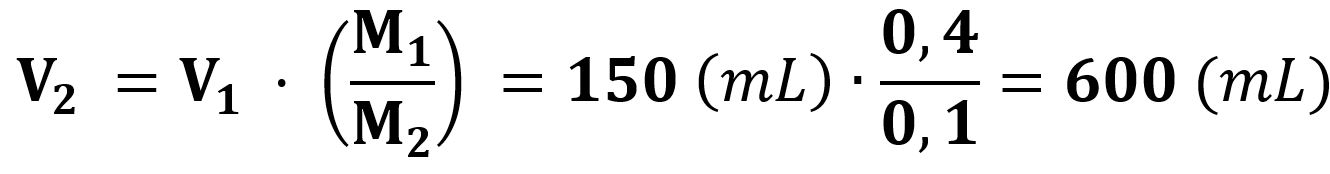 Il volume finale è di 600 mL.
Il volume finale è di 600 mL.
Il quiz non richiede però il volume finale, ma la quantità di acqua da aggiungere per arrivare a questo volume finale. L’acqua da aggiungere è perciò:
600 ‒ 150 = 450 mL
Nota (*):
Quando effettuiamo una diluizione aggiungendo solvente, la quantità di soluto rimane invariata ed aumenta il volume del solvente.
Quantità di soluto iniziale in moli : n1 = M1 · V1
Quantità di soluto finale in moli : n2 = M2 · V2
La formula per calcolare una diluizione si ottiene ponendo la quantità di soluto costante prima e dopo la diluizione:
M1 · V1 = M2 · V2


