Veterinaria 2013
Il sodio (Na) precede il potassio (K) nel Gruppo 1 della tavola periodica. Quale/i delle seguenti affermazioni è/sono corretta/e relativamente a questi due elementi?
- Un atomo di sodio è più grande di un atomo di potassio
- Il potassio è più reattivo del sodio
- Entrambi formano ioni 2+ in composti presenti in natura
- Entrambi hanno una configurazione elettronica esterna s2p1
Bisogna immediatamente inquadrare i due elementi chimici sodio Na e potassio K nella tavola periodica degli elementi. Come dice il testo appartengono al primo gruppo, detto dei metalli alcalini.
Gli elementi del primo gruppo possiedono tutti un solo elettrone nel guscio di valenze e di conseguenza la configurazione elettronica termina per tutti con s1.
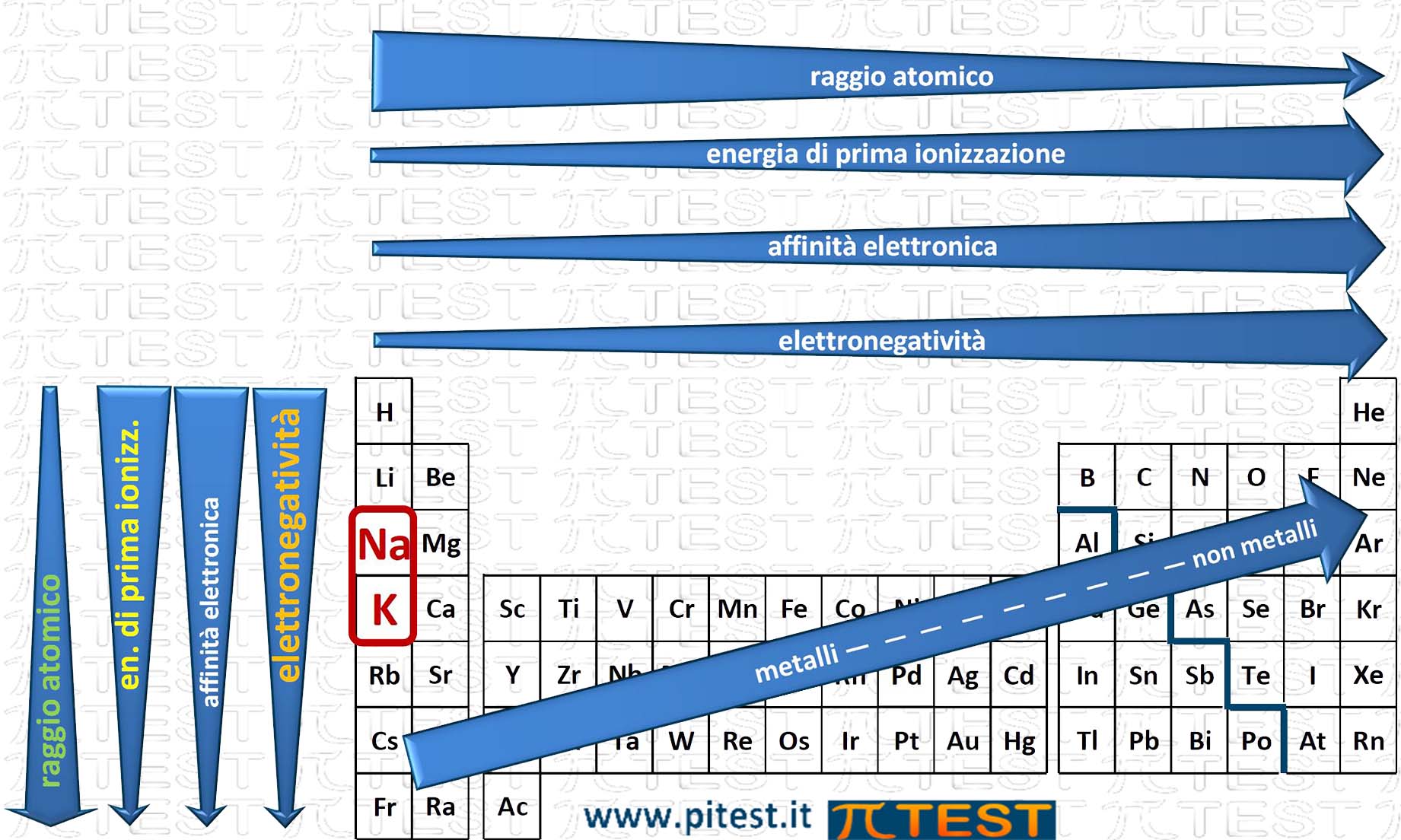
Dobbiamo conoscere l'andamento delle grandezze periodiche nella tavola periodica (vedi la teoria).
Analizziamo ora le quattro affermazioni presenti nel quiz:
1) Un atomo di sodio è più grande di un atomo di potassio
Affermazione ERRATA. Si vede nello schema della figura che il sodio ha raggio atomico più piccolo del potassio.
2) Il potassio è più reattivo del sodio
Parlare di reattività degli elementi chimici messi a confronto (per esempio quelli di uno stesso gruppo) significa valutare la tendenza che gli elementi chimici hanno a reagire in un certo modo quando vanno a formare certi tipi di composti.
La reazione tipica degli elementi del primo gruppo è quella di ossidarsi cedendo l'unico elettrone presente nel guscio di valenza (o guscio esterno). Il sodio Na 1s2 2s2 2p6 3s1 possiede questo elettrone nel terzo livello mentre il potassio K 1s2 2s2 2p6 3s2 3p6 4s1 possiede questo elettrone nel quarto livello. Per il potassio l'elettrone del guscio di valenza si trova più lontano dal nucleo rispetto a quello del sodio; essendo più lontano risulta anche più facile il suo distacco e più facile e reattiva sarà la reazione.
La reazione:
K → K+ + e–
avviene con più facilità (maggiore reattività) della reazione
Na → Na+ + e–
Possiamo concludere che è CORRETTA l'affermazione 2. Il potassio è più reattivo del sodio
3) Entrambi formano ioni 2+ in composti presenti in natura
Affermazione ERRATA. Gli elementi del primo gruppo tendono a cedere facilmente l'unico elettrone che possiedono nel guscio di valenza andando a formari ioni 1+.
4) Entrambi hanno una configurazione elettronica esterna s2p1
Affermazione ERRATA. la configurazione del guscio di valenza (configurazione esterna) degli elementi del primo gruppo è s1


