4.10 I legami intermolecolari
QUIZ 11
Veterinaria 2015
Date le tre coppie di sostanze indicate di seguito, si identifichi per ogni coppia quale sostanza presenta forze intermolecolari maggiori.
1. CH4 e CBr4
2. N2 e NO
3. CH3CH2CH2NH2 e (CH3)3N
[Si assumano temperatura e pressione standard (STP)]
Ricordiamo i tipi di forze intermolecolari e le relative forze di legame.
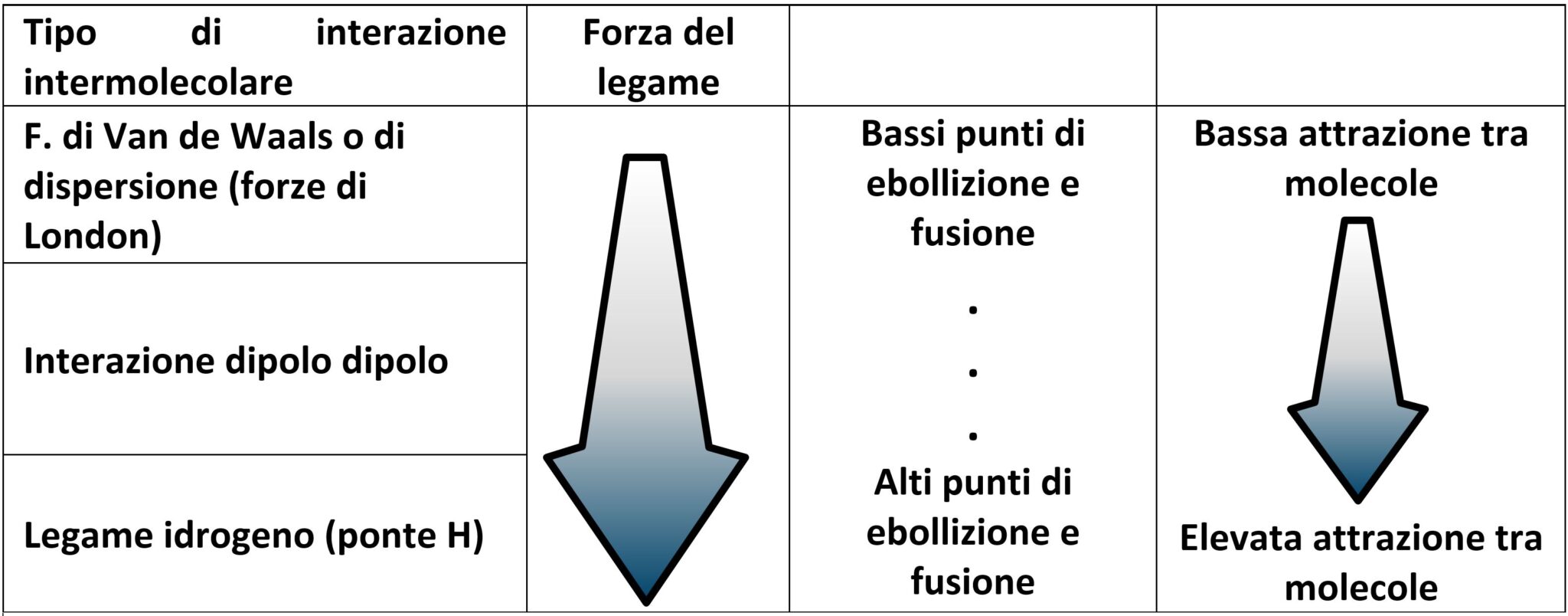
Ragioniamo sul confronto tra le coppie di sostanze proposte nel quiz.
1. CH4 e CBr4
Risulta molto difficile per uno studente stabilire quale dei due composti presenta maggiori forze intermolecolari. Entrambi i composti presentano una perfetta simmetria tetraedrica che annulla i quattro dipoli di legame e rende apolari i due composti. Le forze di interazione intermolecolari saranno perciò per entrambi solamente forze di London. CBr4 è una molecola con peso molecolare molto più alto di CH4 e di conseguenza le forze di Van der Waals saranno più forti.
CBr4 possiede forze intermolecolari più forti di CH4.
2. N2 e NO
L'azoto gassoso N2 è una sostanza pura e il legame tra i due atomi di azoto è omopolare. La molecola risulta apolare. Al contrario NO è costituito da due atomi diversi con diversa elettronegatività e la molecola risulta polare.
NO, polare, possiede forze intermolecolari di tipo dipolo-dipolo più forti rispetto a N2 che possiede solo forze di Van der Waals.
3. CH3CH2CH2NH2 e (CH3)3N
La propilammina CH3CH2CH2NH2 è una ammina primaria. La trimetilammina (CH3)3N è una ammina terziaria.
Le ammine derivano da una molecola di ammoniaca NH3 nella quale uno, due o tre atomi di idrogeno sono sostituiti da radicali organici. L'ammoniaca forma legami intermolecolari a ponte idrogeno tra un atomo di idrogeno e l'atomo di azoto della molecola adiacente. Di conseguenza anche le ammine primarie e secondarie che possiedono ancora un atomo di idrogeno attaccato all'azoto formano legami a ponte idrogeno. Questo non avviene nelle ammine terziarie nelle quali non esistono più atomi di idrogeno attaccati all'azoto.
CH3CH2CH2NH2 possiede forze intermolecolari di tipo a ponte idrogeno più forti di (CH3)3N.
Risulta così corretta la risposta B) che indica CBr4, NO e CH3CH2CH2NH2 .
QUIZ sui Legami Intermolecolari |
|||
|---|---|---|---|
© il testo è di esclusiva proprietà dell’autore ed è sottoposto a COPYRIGHT – non è consentito alcun utilizzo diverso dallo studio gratuito degli utenti del sito


